Basis Roestvast staal les 2
9. Enkele metallurgische principes
De mechanische eigenschappen en dus de fabricage en het gebruik van een metaal of legering hangen af van zijn toestand, dat wil zeggen zijn inwendige structuur. Het is deze inwendige structuur die op zijn beurt niet alleen afhangt van de samenstelling, maar ook van de voorafgaande vervorming en warmtebehandeling.
9.1 Structuur van metalen
Vaste metalen zijn kristallijn, dat wil zeggen hun atomen zijn op regelmatige wijze gestapeld. Van de vele atoomstapelingen die voorkomen in metalen, hoeven er hier maar twee te worden beschreven. De eerste stapeling wordt kubisch ruimtelijk gecentreerd (afgekort k.r.g.) rooster genoemd en is weergegeven op afbeelding la, waar een eenheidscel in deze stapeling is te zien. De tweede stapeling wordt kubisch vlakkengecentreerd (afgekort k.v.g.) rooster genoemd, waarvan de eenheidscel is weergegeven op afbeelding lb. De diameter van een ijzeratoom bedraagt ongeveer 2,3 x 10-8 cm. Dus een heel klein stukje ijzer dat nog zichtbaar is bevat miljarden meer atomen dan er mensen op aarde zijn. Dit zeer grote aantal atomen, dat statistische fluctuaties vereffent, maakt het gedrag van vast metaal met redelijke afmetingen goed voorspelbaar. In een enkel kristal ijzer bij temperaturen beneden 910°C zijn de ijzeratomen gerangschikt volgens het kubisch ruimtelijk gecentreerd rooster. Deze structuur staat bekend als alfa-ijzer of ferriet. Tussen 910° en 1400°C zijn de ijzeratomen gerangschikt volgens het kubisch vlakkengecentreerd rooster, dat bekend staat onder de naam gamma-ijzer of austeniet.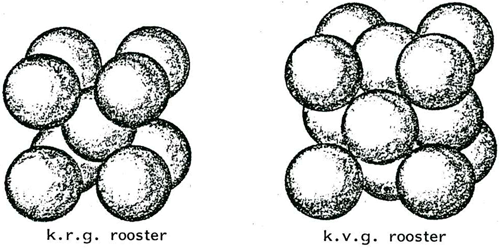
Afb. 1 a) Kubisch ruimtelijk gecentreerd (k.r.g.) rooster.
b) Kubisch vlakken gecentreerd (k.v.g.) rooster.
Tussen 1400°C en de smelttemperatuur (1540°C) gaat het ijzer weer over in het kubisch ruimtelijk gecentreerde rooster, het wordt dan niet meer alfa-ijzer of ferriet genoemd maar delta-ferriet.
Hoewel het voorgaande een redelijke beschrijving geeft van de twee structuren van zuivere ijzerkristallen, moeten er twee complicerende factoren in rekening worden gebracht. De eerste factor hangt samen met het feit dat een brok metaal gewoonlijk bestaat uit heel veel kristallen. Onder de microscoop kunnen die kristallen na een etsbehandeling heel goed zichtbaar worden gemaakt. De structuur van een stuk redelijk zuiver koolstofstaal is te zien op afbeelding 2.
Afb. 2 Microstructuur van redelijk zuiver koolstofstaal.
De afzonderlijke kristallen zijn allemaal opgebouwd uit (voornamelijk) ijzeratomen en het enige verschil is dat hun oriëntaties van elkaar verschillen, zie afbeelding 3.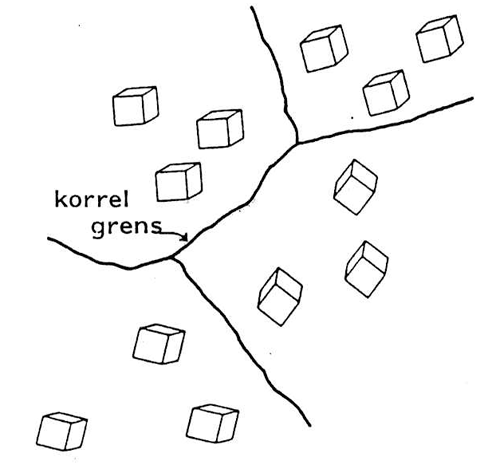
Afb. 3 Oriëntatieverschillen van aan elkaar grenzende kristallen.
Dit verschil in oriëntatie leidt tot wat kristalgrenzen wordt genoemd. Ter plaatse van deze kristalgrenzen, die niet scherp zijn getrokken maar veeleer overgangszones zijn, heerst een zekere mate van wanorde, zie afbeelding 4.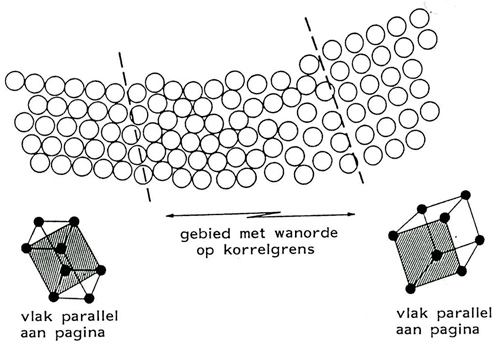
Afb. 4 Atomaire wanorde op een korrelgrens.
Tweedimensionaal verschijnt een kristalgrens in de vorm van een lijn, maar in een driedimensionaal vast stuk metaal zijn kristalgrenzen oppervlakken tussen naburige kristallen. De wanorde van de atomen in deze grensvlakken hangt samen met een uitgesproken reactiviteit. De tweede factor is het gevolg van het feit dat technisch bruikbare metalen zelden zuivere elementen zijn. Zo is roestvast staal een legering van tenminste ijzer en chroom. Er zijn ook nog andere elementen aanwezig. Zo bestaat een ijzerlegering met 13 gewicht % chroom uit een willekeurig mengsel van ijzer- en chroomatomen. De chroomatomen hebben ongeveer dezelfde afmeting als de ijzeratomen en ongeveer een op zeven atomen in de legering is een chroomatoom. Dit mengsel van atomen in een kristal, waarvan de atomen van het tweede element eenvoudig zijn verdeeld in de structuur van het basiskristal, staat bekend als een vaste oplossing. In het beschreven voorbeeld worden de chroomatomen aangetroffen op plaatsen die anders door ijzeratomen worden ingenomen. De vaste oplos¬sing heet daarom substitutioneel. Koolstof en stikstof worden interstitiële elementen in staal genoemd, omdat hun atoomafmetingen zo klein zijn ten opzichte van het ijzeratoom dat ze in zowel het kubisch ruimtelijk gecentreerde als in het kubisch vlakkengecentreerde kristalrooster tussen de ijzeratomen een plaatsje kunnen vinden. In het kubisch vlakkengecentreer¬de rooster lukt dat beter dan in het kubisch ruimtelijk gecentreerde rooster en daarom is de oplosbaarheid van koolstof en van stikstof in austeniet groter dan in ferriet. Dit wordt geïllustreerd door tabel 4.
Tabel 4. Oplosbaarheid van koolstof en stikstof in a- en g-ijzer.
De oplosbaarheid van koolstof in austeniet kan oplopen tot maximaal 2,04%, terwijl dat in ferriet niet meer is dan 0,2%. Stikstof vertoont dezelfde trend. Het is van belang om op te merken dat de oplosbaarheid van stikstof iets hoger is dan die van koolstof. omdat de atoomstraal van stikstof iets kleiner is dan die van koolstof. Voornoemde gegevens gelden voor zuiver ijzer. In het Fe-Cr- legeringssysteem. zoals dat van roestvast staal, is de oplosbaarheid van interstitiële elementen kleiner, maar ook dan geldt hetzelfde verschil tussen de oplosbaarheid in austeniet en ferriet. In austenitisch roestvast staal bijvoorbeeld varieert de oplosbaarheid van koolstof met de temperatuur en is bij 1100°C en hoger ongeveer 0,1%. Als er meer koolstof aanwezig is dan 0,1% dan kan dat overschot geen plaats vinden in de vaste oplossing en zal zich binden met chroom tot chroomcarbide dat in de vorm van een separate fase precipiteert (uitscheidt). Onder de microscoop kan een vaste oplossing niet worden onderscheiden van een zuiver element (hoogstens door soms een kleurverandering). Afbeelding 5 toont de microstructuuropname van een austenitisch roestvast staal: een vaste oplossing van ijzer, chroom en nikkel. Vergelijk deze opname eens met afbeelding 2.
Afb. 5 Microstructuur van austenitisch roestvast staal.
Als de oplosbaarheid in vaste toestand van een bepaald element wordt overschreden dan ontstaat er, zoals hierboven al is opgemerkt, een tweede fase door de vorming van chroomcarbide. De chroomcarbidemoleculen hebben de neiging om zich uit te scheiden op kristalgrenzen en als ze voldoende volume bezitten kunnen ze onder de microscoop worden waargenomen, zie afbeelding 6. Met dit in gedachten kan een begin worden gemaakt met het krijgen van enig inzicht in de structuur van ferritische en austenitische roestvast-staalsoorten. De ferritische soort heeft de ruimtelijk gecentreerde kubische structuur van alfa- ijzer en al naargelang de samenstelling zijn er tussen de een op acht en een op drie ijzeratomen vervangen door chroomatomen. De structuur bevat ook een klein aantal mangaanatomen alsmede atomen van andere elementen, die alle de plaats innemen van ijzeratomen. Er is ook koolstof aanwezig: sommige koolstofatomen nemen interstitiële plaatsen in tussen de roosteratomen en andere vormen carbiden, die aanwezig kunnen zijn op de kristalgrenzen of (en dit hangt af van de voorgeschiedenis van de legering) verdeeld binnenin de kristallen.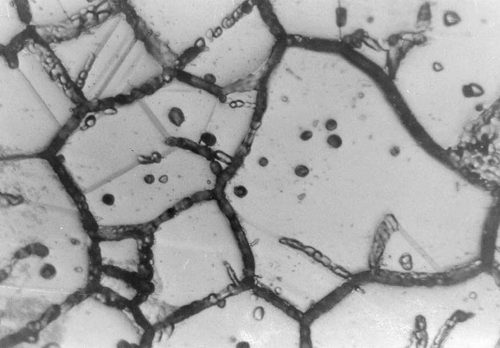
Afb. 6 Chroomcarbide uitgescheiden op korrelgrenzen.
Bij de austenitische soort zorgt toevoeging van nikkel voor de stabilisering van de vlakkengecentreerde kubische structuur (die voor zuiver ijzer stabiel is tussen 1400° en 910°C) tot bij kamertemperatuur. In de gewone legering met rond de 18% chroom en 8% nikkel zou een atoomrangschikking worden verwacht zoals afgebeeld op afbeelding I b, maar dan met ongeveer een op elke vijf atomen een chroomatoom en op ongeveer een op dertien atomen een nikkelatoom, dus een substitutionele vaste oplossing van chroom en nikkel in ijzer. Ook nu zijn er atomen van andere elementen aanwezig. Koolstof bevindt zich weer in ruimten tussen de atomen, maar kan ook carbiden vormen, afhankelijk van de voorgeschiedenis van de legering.
9.2 Hardingsmechanismen
Zuiver ijzer heeft een zeer lage rekgrens. IJzer kan worden gelegeerd met verschei¬dene interstitiële elementen en door een combinatie van enkele hardingsmechanismen kan dit resulteren in een breed scala van mechanische sterkten met bruikbare technische eigenschappen. Er bestaan enkele basismechanismen om staal te harden. De belangrijkste daarvan zijn: vervormingsharding (deformatieharding), martensietharding, oplosharding door interstitiële respectievelijk substitutionele legeringselementen, korrelverfijning en precipitatieharding, ook wel uitscheidingsharding of veroudering genaamd.
9.3 Deformatieharding
Als een metaal of legering plastisch, dat wil zeggen blijvend, wordt vervormd door buigen, knijpen, hameren of enige andere handeling waarbij de rekgrens wordt overschreden, wordt het harder en sterker, tegelijkertijd neemt de taaiheid af. Dit effect, deformatieharding, gaat gepaard met een vervorming van de kristallen en onder de microscoop heeft de deformatiegeharde structuur het uiterlijk van afbeelding 7. De oorspronkelijke eigenschappen van het metaal kunnen worden hersteld door het metaal te verhitten boven de rekristallisatietemperatuur. Sommige metalen, en lood is er zo een, hebben een rekristallisatietemperatuur die ongeveer samenvalt met de kamertemperatuur, vandaar dat ze bij kamertemperatuur niet hardbaar zijn door deformatie. De rekristallisatietemperatuur hangt af van de mate van plastische vervorming, de zuiverheid van het metaal en toevoeging van legeringselementen. Hoe hoger de mate van plastische vervorming, des te lager is de rekristallisatietemperatuur. Toevoeging van legeringselementen daarentegen verhoogt de rekristallisatietemperatuur.
De kristalstructuur beïnvloedt eveneens de deformatieharding: een austenietstructuur geeft snellere deformatieharding dan een ferrietstructuur. Zuiver ijzer kan al rekristalliseren bij 150°C; austenitisch roestvast staal begint pas te rekristalliseren bij ongeveer 700°C. Verschillende legeringen reageren elk op hun eigen manier op koude deformatie. Soms gaat een aanzienlijke sterktetoename samen met een veroudering van kristalstructuur. Als sommige austenitische roestvast-staaltypen bijvoorbeeld koud worden bewerkt, dan heeft de vlakkengecentreerde kubische rangschikking van de atomen de neiging om over te gaan in de ruimtelijk gecentreerde kubische structuur. Dit verschijnsel veroorzaakt een uitgesproken stijging van de hardheid en de sterkte. Als een metaal wordt bewerkt boven zijn rekristallisatietemperatuur dan wordt er gezegd dat het warm wordt bewerkt en dan mag worden aangenomen dat er een simultaan proces plaatsvindt van vervorming en rekristallisatie.
Afb. 7 Microstructuur van gedeformeerd roestvast staal.
9.4 Martensietharding
Als een stuk staal wordt verhit en dan in water wordt ondergedompeld, dan is de hardheid ervan toegenomen. Dit harden hangt samen met een verandering van de kristalstructuur van vlakkengecentreerd kubisch naar een gewijzigde structuurvorm, maar de hardheidstoename wordt teweeggebracht door de koolstofatomen. In grote lijnen komt dat op het volgende neer: het koolstofatoom heeft in het austeniet redelijk de ruimte (de vlakkengecentreerde kubische stapeling van ijzer kan tot ongeveer 1 gewichts-% koolstof herbergen in de ruimten tussen de atomen, met of zonder chroom). Als de legering wordt afgekoeld en de ijzeratomen hun ruimtelijk gecentreerde kubische rangschikking innemen, zitten de koolstofatomen niet meer zo comfortabel, omdat de ruimten tussen de ijzeratomen niet langer groot genoeg zijn om het koolstofatoom te herbergen. Bij langzaam afkoelen kleeft de koolstof vast aan de omringende atomen en vormt waar het kan carbiden en uitscheidingen. Als de afkoeling heel snel gaat is er geen tijd voor de koolstofatomen om carbiden te vormen die zich vervolgens uitscheiden: ze zijn gevangen in de nieuw gevormde ruimtelijk gecentreerde kubische structuur waarin ze niet zo makkelijk zijn onder te brengen.
Daarom is de structuur sterk vervormd door de aanwezigheid van de koolstofatomen en deze vervorming brengt een toename van de hardheid en de sterkte teweeg. De snel afgekoelde structuur staat bekend als martensiet. De afkoelsnelheid die nodig is om zo'n structuur te produceren hangt af van de samenstelling van de legering: in het algemeen geldt dat hoe meer legeringselement er aanwezig is des te langzamer de afkoelsnelheid kan zijn om martensiet te produceren. Bij de samenstelling van roestvast staal is afkoelen in lucht al vaak voldoende om de harde, martensitische structuur te vormen. De feitelijke hardheid die wordt bereikt hangt echter volledig af van de hoeveelheid koolstof in het staal: hoe meer koolstof. des te harder en sterker, maar des te brosser ook wordt dan het staal na harden. Martensitisch materiaal is gewoonlijk niet taai genoeg, vooral als het koolstofgehalte veel hoger is dan 0,1%. Om de taaiheid te verbeteren wordt het staal ontlaten: daarbij wordt het verhit zodat de martensiet uiteen begint te vallen en sommige koolstofatomen de gelegenheid vinden om carbiden te vormen. Dit alles heeft tot resultaat dat de vervorming van de kristallen afneemt. Dit gaat ten koste van de mechanische sterkte.
9.5 Oplosharding in vaste toestand door interstitiële atomen
Koolstof en stikstof zijn de twee elementen die voor een aanzienlijke toename kunnen zorgen van de sterkte van ijzer en aldus van ijzer staal maken. De oplosbaarheid van deze beide elementen is zoals al eerder gezegd hoger in austeniet dan in ferriet. Dit vormt de grondslag voor martensietharding, hetgeen al is behandeld. In staal waarvan de austeniet stabiel is bij kamertemperatuur kunnen koolstof maar vooral stikstof in vaste oplossing de sterkte aanzienlijk verhogen.
9.6 Oplosharding in vaste toestand door substitutionele atomen
De verschillende elementen die met ijzer vaste oplossingen kunnen geven verhogen de sterkte in verschillende mate. Het is echter geen erg krachtig hardingsmechanisme van staal bij kamertemperatuur.
9.7 Korrelverfijning
Verfijning van de korrelgrootte vormt een belangrijk verstevigingsmechanisme voor staal en het is vooral zeer bruikbaar voor ferritisch roestvast staal. Aangezien geldt dat de rekgrens hoger is naarmate de korrelgrootte fijner is, wordt bij de moderne staalbereiding de uiteindelijke ferrietkorrelgrootte nauwkeurig onder controle gehouden.
9.8 Precipitatieharding
Het verschijnsel precipitatieharding, ook wel uitscheidingsharding of veroudering genoemd, komt veel voor bij aluminiumlegeringen. Het algemene principe is het produceren van een sterk onderkoelde vaste oplossing waar tijdens verouderen verbindingen uitscheiden. Net zoals het mogelijk is om een vloeibare oplossing van zout in water sterk te onderkoelen door snel en voorzichtig af te koelen, zo kan ook een sterk onderkoelde vaste oplossing worden verkregen. Bij kamertemperatuur hebben we dan een vaste oplossing die niet stabiel is. maar metastabiel: er zijn meer atomen van legeringselementen in oplossing dan de structuur in werkelijkheid kan herbergen. Als de structuur de gelegenheid hiervoor krijgt dan zullen deze overtollige atomen een aparte fase kunnen vormen. Deze gelegenheid wordt gevormd door de tijd en kan worden bevorderd door toevoer van wat warmte. Gedurende de beginstadia van het precipitatieproces komen de overtollige atomen van hun plaats en gaan zich met andere omringende atomen combineren. Na verloop van tijd zullen ze precipitaten vormen die onder de microscoop zichtbaar zijn. Het is echter gedurende de vroege stadia, voordat de precipitaten zichtbaar zijn, dat de grootste sterktetoename optreedt: dus tijdens wat genoemd wordt het precipitatiestadium. Als er zichtbare precipitaten zijn ontstaan is de sterkte gewoonlijk op zijn retour en heet de legering oververouderd
De precipitaten die samengaan met het hardingsproces zijn zeer complex van structuur. Bij precipitatiehardend roestvast staal worden elementen (aluminium, molybdeen, koper) toegevoegd die werkzaam zijn in het precipitatiehardingsproces en ze ondergaan speciale warmtebehandelingen om de eerste oververzadigde vaste oplos¬sing te produceren alsmede ten behoeve van het daarop volgende precipitatiestadium.
10. Warmtebehandelingen
10.1 Zachtgloeien
Het doel van zachtgloeien is het metaal in de zachte toestand brengen. Deze behandeling moet niet worden verward met ontlaten, dat een onlosmakelijk onderdeel vormt van de dubbele behandeling die bestaat uit afschrikken en ontlaten en die is bedoeld om een gewenste combinatie te verkrijgen van sterkte en taaiheid in een hardbaar staal. Zachtgloeien is voor elk materiaal weer anders. Zo kan martensitisch roestvast staal worden zachtgegloeid door het te verhitten boven de kritische temperatuur, dus tot in het austenietgebied, en dan zo langzaam af te koelen, dat er in plaats van martensiet ferriet ontstaat. Ook mogelijk is zachtgloeien door te verhitten tot even onder de kritische temperatuur waarbij de eerder gevormde martensiet uiteenvalt. De bedoeling is niet het verkrijgen van een bevredigende combinatie van sterkte en taaiheid, zoals dat wel het geval is bij afschrikken en ontlaten, maar puur en alleen het in een zachte toestand brengen. Zachtgloeien bij hogere temperaturen geeft een zachter metaal. Bij austenitisch en ferritisch roestvast staal is er geen duidelijk waarneembaar verschil tussen zachtgloeien boven en even onder de kritische temperatuur. Omdat austenitisch roestvast staal niet kan worden gehard via de martensietomzetting, heft zachtgloeien de hardheid op die is ontstaan door koudvervormen. Zachtgloeien kan ook zorgen voor het weer in oplossing doen gaan van chroomcarbiden die zich op de korrelgrenzen hebben afgezet of binnenin de korrels van austenitisch roestvast staal. In dat geval wordt er ook wel gesproken van oplosgloeien.
10.2 Spanningsarmgloeien
De warmtebehandeling die wordt aangeduid als spanningsarmgloeien (er wordt ook wel gesproken van spanningsvrijgloeien) is in feite een zachtgloeibehandeling. De bedoeling van spanningsarmgloeien is niet het zachtmaken van het staal (hoewel dat natuurlijk wel kan gebeuren), maar het verlagen van mechanische restspanningen die in het materiaal zijn geïntroduceerd tijdens vormgeving en/of laswerkzaamheden.
10.3 Homogeengloeien
Bij het homogeengloeien wordt het materiaal op een dusdanig hoge temperatuur gebracht dat de atomen zich met een redelijke snelheid in het metaal kunnen verplaatsen (diffunderen). Met deze gloeibehandeling kunnen verschillen in uitscheidingen worden vereffend, hetgeen vooral wenselijk is bij precipitatiehardende roestvast-staaltypen. De gloeitemperatuur bedraagt 1100°C. Austenitisch roestvast stalen gietstukken moeten na een homogeengloeiing snel worden afgekoeld.
10.4 Nitreren
Met nitreren kunnen dunne, maar zeer harde oppervlakken worden verkregen met uitstekende slijtvastheid en verbeterde vermoeiingseigenschappen. Het proces bestaat in principe uit het onderwerpen van het werkstuk aan een actieve stikstofhou¬dende atmosfeer, gewoonlijk ammoniak, bij ongeveer 540°C. Nadien hoeft niet te worden afgeschrikt. De respons op het nitreren hangt af van de legeringssamenstelling. Roestvast staal kan, voornamelijk door zijn chroomgehalte, worden genitreerd (de austenitische typen heel moeilijk) en er ontstaat gedurende een 48 uur durende behandeling een laag met een dikte tussen 0,1 en 0,2 mm. Na deze periode neemt de laagdikte nauwelijks toe, zodat een behandeling langer dan 48 uur weinig effect sorteert. Alvorens te gaan nitreren moet het werkstuk spanningsarm worden gegloeid en het nitreren moet de laatste warmtebehandeling zijn in geval er meer dan één warmtebe¬handeling wordt gegeven. Er ontstaat wat aangroei als gevolg van de vorming van de nitridelaag en er zijn wat experimenten nodig om nauwkeurig te kunnen vaststellen welke vormveranderingen onder gegeven omstandigheden zijn te verwachten. Het roestvast-staaloppervlak moet worden gedepassiveerd door een reductieproces of enige andere geschikte methode om een oxidelaag te verwijderen en absolute reinheid is essentieel. Genitreerde roestvast stalen onderdelen worden onder andere met succes toegepast voor klepstelen, assen, lagers en vezelgeleiders. De corrosieweerstand van het roestvaste staal neemt als gevolg van de nitreerbehandeling aanzienlijk af en om deze reden moet het gedrag ervan in corrosieve milieus proefondervindelijk worden vastgesteld.
10.5 Praktische kanten
Eisen ten aanzien van warmtebehandeling beginnen met een grondige reiniging van de werkstukken. Sporen van organisch materiaal, vingerafdrukken, potloodstrepen moeten volledig worden verwijderd. Rekken voor in de ovens moeten van materiaal zijn gemaakt, dat het te behandelen roestvast staal niet verontreinigt. In het algemeen wordt voor dat doel gebruik gemaakt van roestvast staal of van een hittevaste nikkel-legering.
Het verhitten kan plaatsvinden in een oven, zoutbad, inductiespoel of open vlam. Dat laatste beperkt zich tot verhitten met een toorts als onderdeel van een lascyclus. Zachtgloeien door middel van inductie is ook toepasbaar voor het warmtebehandelen van lassen en het is in het bijzonder geschikt bij continue productie of bij een opeenvolgende reeks van individuele stuks. Ovens en zoutbaden komen echter het vaakst voor.
Ovens
Verhitten kan plaatsvinden met branders of met gloeidraad. Roestvast staal wordt gewoonlijk verhit in een atmosfeer bestaande uit lucht en de oxidehuid wordt naderhand verwijderd door te beitsen. De mate van oxidevorming kan in open ovens worden beperkt door beheersing van het lucht-brandstofmengsel en het gevaar voor opkoling wordt vermeden door te zorgen voor voldoende vrije zuurstof in de atmo¬sfeer.
Extern opgewekte atmosferen van het endotherme soort voldoen meestal niet als gevolg van hun neiging tot opkoling. Verder kan hun waterstofgehalte leiden tot verbrossing van de martensitische roestvast-staaltypen. Atmosferen van het exotherme type voldoen wel, maar veroorzaken soms wat oxidevorming.
Om volledige inertie te verkrijgen kan gebruik worden gemaakt van argon of van helium, maar de hoge kosten daarvan zijn zelden te rechtvaardigen. Vandaar dat voor blankgloeien gewoonlijk gedissocieerde ammoniak wordt gebruikt. Om nitreren te vermijden, moet de ammoniak zijn gedissocieerd bij een hoge temperatuur: 980°C vertegenwoordigt een redelijk compromis tussen een zo volledig mogelijke dissocia¬tie met een economische snelheid en aantasting van de apparatuur. Het gas dat voor blankgloeien wordt toegepast moet droog zijn. Dauwpunten met waarden van niet lager dan -60° tot -75°C zijn aan te bevelen. Temperatuurbeheersing, noodzakelijk bij alle warmtebehandelingsprocessen, is van bijzonder gewicht bij warmtebehandeling van roestvast staal, omdat bevredigende temperatuursstrajecten dikwijls worden ingeperkt door pogingen om verbrossing of sensitisering te vermijden. Waterstofverbrossing kan optreden in de martensitische roestvast-staaltypen als gevolg van het opnemen van waterstof in de oven. Dit ver¬schijnsel treedt gewoonlijk niet op als de afkoelsnelheid tamelijk laag is en als het optreedt kan het worden opgeheven door ontlaten bij een betrekkelijk lage temperatuur.
Zoutbaden
Warmtebehandeling van martensitisch roestvast staal kan heel goed plaatsvinden door de werkstukken te verhitten in gesmolten zout. Advies over geschikte zouten, containers en verhittingsmethoden kan het best worden ingewonnen bij leveranciers. Zouten die meestal worden gebruikt zijn natriumcarbonaat of bariumchloride (waarschijnlijk met toevoeging van nog andere chloriden). Het zoutbad waarin roestvast staal wordt verhit moet bij voorkeur niet voor nog andere metalen worden gebruikt, teneinde problemen met verontreiniging te voorkomen.
Behandeltijden kunnen het beste proefondervindelijk worden vastgesteld. Zodra het werkstuk uit het zoutbad wordt gehaald moet het zo snel mogelijk grondig van alle zout worden ontdaan. Zoutbaden kunnen uiteraard ook worden gebruikt voor zachtgloeien: of er een zoutbad wordt genomen of een oven is een economische beslissing.



