Aluminium in voedsel en milieu
De mensheid ontwikkelde zich onder andere door gebruik te maken van primitieve biochemicaliën en sporen metalen die op het aardoppervlak werden aangetroffen. Over het algemeen ging het om elementen die makkelijk te vinden waren. Dit was een langgerekt proces dat meer dan 4,5 miljard jaar geleden een aanvang nam. Hoewel het op twee na het meest voorhanden element is in de aardkorst, wist aluminium zich op grond van zijn chemische aard op effectieve wijze te onttrekken aan biochemische en stofwisselingsprocessen. Dit is voor een groot deel het gevolg van de lage oplosbaarheid van aluminiumsilicaten, -fosfaten en -oxiden, waardoor het aluminium chemisch niet beschikbaar was.
Gelet op deze feiten zijn de volgende observaties te verklaren:
- Er is geen actief of specifiek pad voor de opname en het vasthouden van aluminium in het menselijk organisme.
- De twee meest voorkomende elementen in de lithosfeer (gesteenten) zijn zuurstof en silicium. Het is dan ook niet verwonderlijk dat aluminium gewoonlijk wordt aangetroffen in de natuur in de vorm van silicaten, waardoor het nauwelijks in chemisch en biologisch actieve toestand voorhanden is.
- Gezien het voorgaande is het hoogst onwaarschijnlijk dat aluminium een factor van belang is bij de voedsel opname. Directe bewijzen hiervoor zijn echter moeilijk te verkrijgen vanwege de talrijke moeilijkheden om aluminiumvrije diëten voor experimentele doeleinden te produceren.
Aluminium en het milieu
Aluminium is niet alleen alomtegenwoordig in grote hoeveelheden in ons milieu, maar ook het brede scala van technologische toepassingen die voor aluminium zijn gevonden heeft geresulteerd in een enorm wereld verbruik. Zonder aluminium zouden onze bouwwerken niet functioneren, moderne vliegtuigen zouden niet kunnen opstijgen en talloze ongemakken zouden zich dan manifesteren. De ingebouwde veroudering die samengaat met verbruiksgoederen betekent dat bovenop het al aluminiumrijke milieu waarin wij leven, het als afval storten van aluminium en aluminiumhoudende goederen nog meer toevoegt aan de last die de mens moet torsen. Het is paradoxaal dat, omdat overal waar we kijken zulke grote hoeveelheden aluminium aanwezig zijn, analyse op betrekkelijk lage concentraties aluminium in ons voedsel of drank buitengewoon zorgvuldig handelen vereist alsmede het gebruik van een smetvrije ruimte. Deze moeilijkheid bij het meten van microconcentraties in een megaconcentratieomgeving is deels verantwoordelijk voor de late ontdekking dat aluminium een gezondheidsrisico vormt, hetgeen pas in 1970 werd geopenbaard toen het nu welbekende verband werd gelegd tussen hoge aluminiumniveaus in leidingwater voor nierdialyseapparatuur enerzijds en met de opeenhoping van het element in menselijk hersenweefsel en mogelijk met dialysedementie anderzijds.
Stofwisseling
Het schema toont de diverse wegen waarlangs aluminium vanuit de omgeving het menselijk lichaam kan binnendringen en wel via ons voedsel, via toevoegingen aan voedingsmiddelen, via gezondheids- en medicinale preparaten en via het toedienen van aluminium als middel tegen zuur, tegen diarree, of als een anti - fosfaat absorberend middel uit het maagdarmkanaal. Aluminium biedt een klassiek voorbeeld dat door voedingsdeskundigen wordt aangehaald om de verschillen te onderstrepen tussen ingang en opname. Evolutieprocessen hebben samengewerkt om aluminium uit de mens te weren.
- 1: aluminiumertsen in de geosfeer hebben het element krachtig gebonden in de vorm van silicaten.
- 2: vrijgemaakt aluminium raakt bedekt met een inerte oxidelaag, die het metaal resistent maakt tegen corrosie.
- 3: aluminium ionen in ons dieet worden niet door de dunne darm opgenomen en komen niet in de bloedbaan te recht.
Die metaalionen die niet aanwezig zijn in de vorm van kationen kunnen complexe verbindingen aangaan met liganden met lage molecuulmassa’s (liganden kunnen bestaan uit eenvoudige negatieve ionen zoals Cl- of OH- complexe negatieve ionen zoals ethyleendiaminetetra-acetaat of kort weg EDTA, maar ze kunnen ook uit neutrale moleculen bestaan zoals water of NO). Ten slotte: als kleine hoeveelheden aluminium in het bloedplasma te rechtkomen dan wordt het niet doorgeleid door weefsels waarin het kan worden vast gehouden en waardoor de normale biochemische toestand veranderen, maar zulke geladen ionen worden snel uitgescheiden via de normale nierfuncties. Als echter een of meer van deze beveiligingen wordt omzeild zoals bijvoorbeeld het geval is bij directe inspuiting van vloeistoffen in de bloedbaan, door onvoldoende nierwerking, of omdat aluminiumstof de longen binnendringt, kan aluminium een bedreiging vormen voor onze normale stofwisselingsprocessen. Studies hebben echter aangetoond dat onder fysiologische omstandigheden de oplos baarheids- en ladingskarakteristieken van het element van dien aard zijn dat een dergelijke bedreiging gering blijft.
Chemische overwegingen
De ionstraal van Al3 + komt sterk overeen met die van Fe3 + en zijn neiging om zich met een watermantel te omgeven in waterige oplossingen vertoont overeenstemming met die van Fe3 +. Het kation [Al(H2O)6]3 + is alleen stabiel in zure oplossingen, zo dat bij pHwaarden hoger dan 3 hydrolyse optreedt waarbij [Al(H2O)5(OH)]2 + en [Al(H2O)4(OH)2]+ ontstaan. De vorming van Al(OH)3 dicteert de grens van de oplosbaarheid van aluminium (bij ongeveer pH 6,5) en bij nog hogere waarden ontstaat het aluminiumnitraation Al(OH)4 -. Bij pH 7,4 is er overwegend sprake van Al(OH)4 -.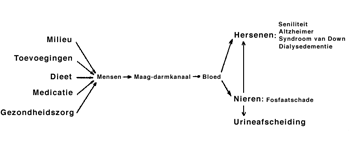
Schema Wegen die aluminium kan volgen in het menselijk gestel.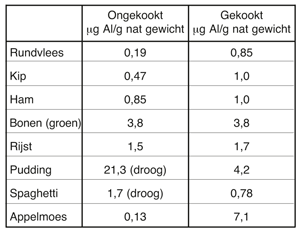
Tabel 1 Aluminiumgehalte van voedingsmiddelen voor en na koken in aluminium pannen.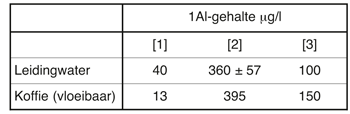
Tabel 2 Aluminiumgehalte van koffie die is gezet in geheel van aluminium gemaakte koffiemachines.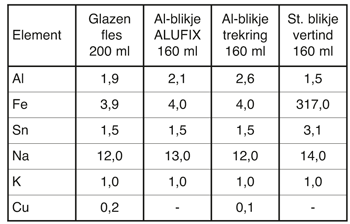
Tabel 3 Gehalte in mg/l aan verscheidene elementen in witte wijn
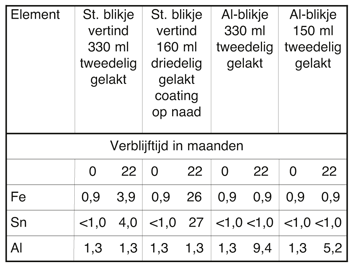
Tabel 4 Gehalte in mg/l aan Fe, Sn en Al in appelmoes, verpakt in verschillende houders na 0 en na 22 maanden opslag [4].
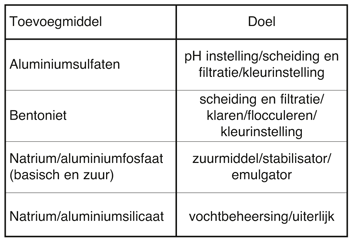
Tabel 5 Aluminium in toevoegmiddelen voor voedingswaren.
Aluminium in contact met voedingsmiddelen
Voedingsmiddelen met neutrale activiteit en laag zoutgehalte tasten aluminium met daarop een natuurlijke oxidelaag niet noemenswaardig aan. Aluminium gedraagt zich gelijkelijk in contact met melk, natuurlijke melkproducten, eetbare oliën en vetten bij omgevingstemperatuur. Glucose, eiwitten en pectine fungeren als inhibitoren in producten die vruchtenzuren bevatten. In de VS zijn aluminiumgehaltes geanalyseerd in voedingswaren die zijn gekookt in pannen, gemaakt van ongelegeerd aluminium (zie tabel 1). Er werd geconstateerd dat de hoeveelheid aluminium die overging naar het voedsel als gevolg van het koken in het aluminium gerei minder dan 0,1 mg aluminium per 100 g bedroeg voor de meeste etenswaren. In het geval van appelmoes liep deze hoeveelheid op tot 0,7 mg. De conclusie was dat de hoeveelheid aluminium die tijdens het koken in ongelegeerd aluminium kookgerei in het eten terechtkwam klein is vergeleken met de verschillen in het aluminiumgehalte van voedingsmiddelen die het gevolg zijn van verschillen in plantensoort, bodemgesteldheid en groeiomstandigheden. Het Zwitserse Instituut voor Technologie te Zürich [2] heeft de opname gemeten van aluminium door koffie in aluminium koffiemachines onder gebruikmaking van water uit verschillende bronnen. De resultaten (zie tabel 2) laten zien dat het aluminiumgehalte van kraanwater in Zürich aanzienlijk kan variëren als gevolg van de behandeling die het heeft ondergaan. Het aluminiumgehalte van de koffie was echter niet of nauwlijks hoger dan dat van het gebruikte kraanwater.
Alcoholica en frisdrank in contact met gecoat aluminium
Om een overzicht te krijgen van migratie van aluminium naar alcoholische drank vanuit gecoate aluminium blikjes is door Alusuisse in samenwerking met het Zwitserse Federale Instituut voor Fruitteelt, Wijnbouw en Tuinbouw te Wadenswil onderzoek gedaan naar het gedrag van witte wijn in verschillende containers [3]. Deze containers waren:
- groenglazen flessen met een inhoud van 200 ml;
- stalen blikjes met een inhoud van 160 ml, voorzien van een inwendige vernislaag;
- aluminium blikjes met een inhoud van 160 ml, voorzien van een inwendige vernislaag en met twee typen sluiting:
- ALUFIX en een treksluiting
De oxidatie en verandering van het gehalte aan metalen en H2S in witte wijn over een periode van twee jaar opslag zijn onderzocht. De witte wijn was een 1983 Riesling Sylvaner uit het kanton Genève. Alle kenmerken van witte wijn zijn geanalyseerd. De pH-waarde bedroeg 3,66, hetgeen vrij laag is. Blikjes en flessen werden gevuld onder gedefinieerde omstandigheden van CO2-atmosfeer en afvulruimte. Blikjes en flesjes werden opgeslagen bij 20 ± 3°C. Smaak- en geur evaluaties en analytisch onderzoek van elke verandering werden uitgevoerd na 1, 7, 26, 52 en 100 weken. De veranderingen in de Al, Fe, Sn, Na, K en Cu gehaltes, gemeten met atoomabsorptiespectrometrie, zijn weergegeven in tabel 3. Het betrekkelijk hoge gehalte aan ijzer en tin in de wijn die is opgeslagen in vertonde stalen blikjes is het gevolg van kleine roestplekjes op de lasnaad van het blikje, dat was bekleed met een tweecomponentenvernis. Het aluminiumgehalte van de wijn in de glazen flessen en stalen blikjes was slechts iets lager vergeleken met het aluminiumgehalte van de wijn in de aluminium blikjes. Alusuisse heeft ook onderzoek gedaan naar de invloed van verschillende soorten verpakkingsmateriaal en opslagtijd op het gehalte aan aldehyden, kationen en metalen in appelsap [4]. Aldehyden en kationen zijn belangrijke geur- en smaakstoffen die aan vruchten en vruchtensap worden toegevoegd en ze beïnvloeden de kwaliteit van dergelijke producten. De resultaten met betrekking tot de metaalgehaltes die zijn vastgesteld in het verse appelsap en na opslag gedurende 22 maanden in verschillende containers zijn interessant (zie tabel 4). De extreem lange opslagtijd van 22 maanden was gekozen met als doel het evalueren van extreme condities die zich in de praktijk niet voordoen. Na 22 maanden was het aluminiumgehalte slechts licht gestegen als gevolg van minuscule corrosielekjes die zijn ontstaan op het vervormde deel van het deksel.
Ten slotte
Uit het voorgaande is gebleken dat aluminium wordt overgedragen van kookgerei en verpakkingsmateriaal in hoeveelheden tot maximaal 10 mg/kg. Deze meetwaarden moeten echter worden gezien tegen de achtergrond van de andere bronnen van herkomst van dit metaal in het menselijk dieet. Zo wordt aluminium op grote schaal gebruikt in een verscheidenheid van toevoegingen aan voedingswaren (zie tabel 5). In de VS wordt voor dit doel jaarlijks zo’n 2000 ton aluminium gebruikt.
Literatuur
1. J.L. Greger, W. Goetz, D. Sullivan. Journal of Food Protection, Vol. 48, Sept. 1985.
2. Ch. Schlatter, A. Kauzig. Untersuchungsbericht des Instituts für Toxicologie der ETH und Universität Zürich, Schwerzenbach 1985.
3. P. Dur, S. Block. Deutsche Lebensmittel-Rundschau, H. 12 1987.



