Corrosie van Roestvast staal Deel 3
Spleetcorrosie is een corrosievorm welke alleen voor kan komen in nauwe ruimten als spleten. Vele constructies bevatten spleten, hierbij kan b.v. aan spleten tussen flenzen in leidingsystemen (zie afb. 1) of spleten welke t.g.v. overlappingsnaden ontstaan worden gedacht. Een mooi voorbeeld van een constructievorm welke vele spleten vertoont is een constructie waaraan gepuntlast is. De overlappingsnaden vormen immers goed gedefinieerde spleten.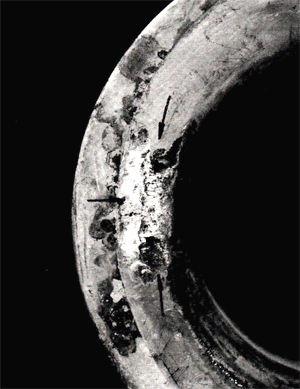
Afb. 1. Aantasting van de flens van een pijpsysteem t.g.v. spleetcorrosie. D.it is een veel voorkomend verschijnsel omdat tussen de pakking en de flens vaak spleten voorkomen (foto: MCE).
Wat is spleetcorrosie?
Spleetcorrosie wordt veroorzaakt door een aantal samenwerkende factoren . Afb. 2 toont een principeschets van het mechanisme achter spleetcorrosie. Typerend voor deze corrosievorm is, dat de kathodische reacties buiten de spleet plaats vinden, terwijl de anodische reacties (het oplossen van het metaal) in de spleet plaatsvinden. Eén van de voorwaarden waaraan voldaan moet worden om spleetcorrosie plaats te laten vinden is, dat het materiaaloppervlak in de spleet en het materiaaloppervlak buiten de spleet elektrisch contact met elkaar moeten maken. Tevens moeten deze oppervlakken in contact zijn met een geleidend medium.
Ten gevolge van corrosiereacties in de spleet, zal het zuurstofgehalte aldaar snel dalen. Het zuurstofgehalte buiten de spleet blijft echter t.g.v. verversing van het medium op normaal peil, waardoor het materiaal buiten de spleet een hogere potentiaal aanneemt.dan het materiaal in de spleet. Het gevolg is, dat ter verhoging van de potentiaal in de spleet, de metaaloplossingsreacties (anodische reacties) versneld plaats gaan vinden, terwijl net buiten de spleet de kathodische reacties de overhand krijgen. Het elektronentransport zal dus van het spleetoppervlak naar het oppervlak buiten de spleet gaan. Om een zeker elektrisch evenwicht te verkrijgen, zullen de positieve ionen in de spleet negatieve chloride-ionen aantrekken, wat inhoudt, dat de agressiviteit van het medium in de spleet aanzienlijk toeneemt. De aanwezigheid van deze chloride-ionen vergemakkelijkt tevens de hydrolyse van water waardoor de volgende reactie plaats vindt:
M+ + Cl- + H2O -->, MOH + H+ + Cl -
waarbij M staat voor een willekeurig Metaalatoom.
Buiten de spleet vindt de al in deel 1 van deze serie vermelde kathodische reactie:
O2 + 2H2 + 4e --> 4OH- (basisch of neutraal milieu)
of
4H+ +O2 + 4e -> 2H2O (zuur milieu)
plaats.
Ten gevolge van de hydrolyse reactie neemt de pH sterk af (tot onder pH 2) [1]. Deze sterke pH-daling is weer een extra factor welke verantwoordelijk is voor het soms zeer snelle verloop van spleetcorrosie. Onder een bepaalde pH-waarde vindt namelijk een overgang van een passief naar een actief oppervlak plaats.
Bepalen van de gevoeligheid voor spleetcorrosie
Elektrochemische technieken
Uit de polarisatiecurve van een passief metaal kunnen bepaalde conclusies betreffende de spleetcorrosiegevoeligheid van dat metaal verkregen worden. De zgn. kritische stroomdichtheid ikrit (afb. 3) is een waarde welke aangeeft hoe gemakkelijk een metaal passiveert.
Een metaal wat gemakkelijk passiveert is minder gevoelig voor spleetcorrosie dan een metaal wat moeilijk passiveert. Ook het verschil tussen de pittingpotentiaal en de repassiveringspotentiaal is een maat voor de spleetcorrosiegevoeligheid. Een klein verschil duidt een gemakkelijke repassivering aan, m.a.w., een doorbroken oxidehuid zal gemakkelijk herstellen.
Afb. 4 toont het verschil tussen de pitting-en repassiveringspotentiaal van verschillende legeringen in zeewater als functie van de corrosiesnelheid, uitgedrukt in gewichtsverlies/tijdseenheid. Hoe kleiner het verschil, hoe bestendiger het materiaal. Een speciaal tegen spleetcorrosie ontwikkelde legering is de Hastelloy alloy C legering (nikkellegering met 1,25% Co, 16% Cr, 17% Mo, 4% W en 5,75% Fe). Deze legering blijkt in zeewater dan ook een minimaal verschil tussen de pittingspotentiaal en de repassiveringspotentiaal op te leveren.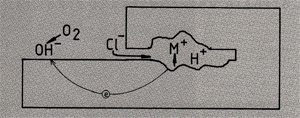
Afb. 2. Principeschets van het mechanisme achter spleetcorrosie. Buiten de spleet vinden de kathodische reacties plaats, waarvan de belangrijkste is:
0, + 2H2O + 4e -->+ 4QH-.
In de spleet lost het metaal op, worden negatieve ionen als chloride-ionen van buiten de spleet aangetrokken en ontstaan H+ -ionen t.g.v. de hydrolyse van water.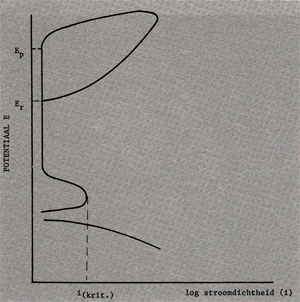
Afb. 3 Polarisatiekromme van een passief metaal. De kritische stroomdichtheid ikrit· en het verschil tussen de pittingpotentiaal Ep en repassiveringspotentiaal Er, zijn een maat voor de spleetcorrosiegevoe/igheid.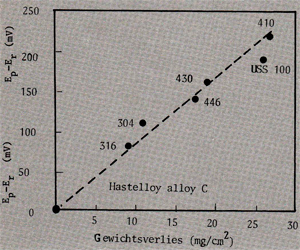
Afb. 4. Verband tussen Ep- Er en de spleetcorrosiesnelheid van verschillende legeringen in zeewater (expositietijd 4,25 jaar). Uit deze grafiek blijkt dat aan de hand van het verschil tussen de pitting- en repassiveringspotentiaal een redelijke uitspraak over de spleetcorrosiegevoeligheid kan worden gedaan [7].
Spleetcorrosietest van Anderson
Bovenbeschreven methoden geven slechts een grove indicatie van de spleetcorrosiegevoeligheid. Er zijn betere testmethoden, ook deze zijn echter niet genormaliseerd. Een feit is, dat spleetcorrosie een kansproces is wat zich moeilijk d.m.v. testen laat vastleggen.
De oorzaak hiervan is, dat moeilijk te definiëren factoren als afmetingen van de spleet, oppervlaktegesteldheid en constante samenstelling van het medium de resultaten aanzienlijk beïnvloeden. Vandaar dat tests op statistische basis het meest voor de hand liggen. De reproduceerbaarheid van één test is over het algemeen gering. Dit betekent dat per test meerdere metingen nodig zijn om significante resultaten te krijgen. Bij de spleetcorrosietest van Anderson [2] worden bovengenoemde problemen ondervangen door vele metingen tegelijkertijd uit te voeren.
De spleten worden gevormd door een teststrip tussen twee gegroefde teflon onderlegringen te klemmen (zie afb. 5). ledere ring heeft b.v. twintig groeven, wat dus inhoudt dat per teststripje veertig spleten beschikbaar zijn. In het algemeen worden voor deze test drie teststripjes gebruikt, wat een totaal van 120 spleten oplevert. Nadat de gevormde spleten gedurende een bepaalde tijd aan een bepaald milieu zijn blootgesteld, worden de ringen losgehaald waarna het aantastingsbeeld bekeken wordt. Afb. 6 laat het aantastingsbeeld van het teststripje zien, voor deze test zijn ringen met 12 groeven gebruikt.
Van elk spleetje wordt de diepte van de eventuele aantasting bepaald waarna deze wordt uitgezet tegen het percentage spleten dat eenzelfde of een diepere aantasting vertoont. Afb. 7 toont een voorbeeld van een dergelijke grafiek, waarbij twee rvs gietlegeringen getest zijn . Uit deze grafiek kan b.v. worden afgeleid dat wat de CA-151egering in zeewater betreft, de kans op het ontstaan van aantastingen dieper dan 1 mm 50% is. Of dat de kans op het ontstaan van spleetcorrosie bij de CF-SM in zeewater ruim 20% is.
Spleetcorrosietemperatuur en depassiverings pH
Andere testmethoden die wel toegepast worden, zijn het bepalen van de zgn. 'spleetcorrosietemperatuur' en het bepalen van de zgn. 'depassiverings pH'.
Bij het bepalen van de spleetcorrosietemperatuur wordt gebruik gemaakt van de temperatuur, of beter gezegd het temperatuursinterval waarbij spleetcorrosie zich begint te manifesteren. In het kort komt het er bij deze testmethode op neer, dat een proefstuk gedurende een bepaalde tijd aan een bepaald milieu op een bepaalde temperatuur wordt blootgesteld. Heeft zich na de vastgestelde tijd nog geen spleetcorrosie geopenbaard, dan wordt de temperatuur verhoogd met b.v. 5° C, waarna weer blootstelling plaatsvindt. Die temperatuur waarbij de spleetcorrosie zich voor het eerst manifesteert wordt de spleetcorrosietemperatuur genoemd. Hoe hoger de spleetcorrosietemperatuur van een bepaald metaal in een bepaald medium, hoe bestendiger dit metaal tegen spleetcorrosie is. Zoals al vermeld, tijdens het spleetcorrosieproces speelt de pH een grote rol. Dit komt doordat bij daling van de pH, het materiaal van de passieve naar de actieve toestand gaat. M.a.w . de beschermende functie van het oxidehuidje verdwijnt. Deze overgang is te meten aan de hand van de corrosiepotentiaal.
Een plotselinge daling van deze potentiaal tijdens pH verlaging geeft aan dat het oppervlak actief wordt. Op deze wijze is het dus mogelijk om de spleetcorrosiegevoeligheid te meten zonder dat er spleten aangebracht moeten worden.
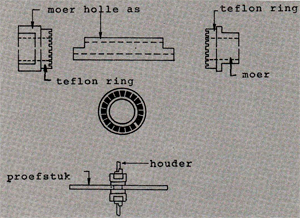
Afb. 5. Proefplaatje met gegroefde onderlegringen.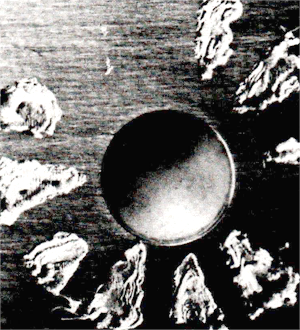
Afb. 6. Kenmerkend aantastingsbeeld dat ontstaat onder gegroefde onderlegringen (foto: MCE).
Invloed van de legeringssamenstelling en microstructuur
Naar de invloed van delegeringssamenstelling op de spleetcorrosiegevoeligheid is relatief weinig onderzoek verricht. Omdat putcorrosie en spleetcorrosie vrij veel overeenkomsten hebben, wordt vaak gesteld dat elementen welke de weerstand tegen putcorrosie beïnvloeden, de weerstand tegen spleetcorrosie op dezelfde wijze beïnvloeden. Chroom, nikkel en molybdeen beïnvloeden de weerstand tegen spleetcorrosie in ieder geval in positieve zin. Verstoringen van microstructuur als delta ferriet, sigma fase, sulfiden en precipitaten zijn spleetcorrosiebevorderend.
Andere factoren
Verhouding tussen oppervlak buiten de spleet en spleetoppervlak
Een factor welke bij spleetcorrosie een grote rol speelt is de verhouding tussen het spleetoppervlak (anode) en het oppervlak buiten de spleet (kathode). Onderzoek heeft aangetoond [3], dat wat rvs-spleten in zeewater betreft, verkleinen van de spleet en / of vergroten van het oppervlak buiten de spleet, het ontstaan van spleetcorrosie in de hand werkt. Dit effect is te vergelijken met galvanische corrosie (zie deel1 van deze serie), waarbij een kleine anode t.o.v. een grote kathode ook ernstige gevolgen kan hebben. Bij een dergelijke verhouding is de stroomdichtheid in het anodeoppervlak immers veel groter, hetgeen inhoudt, dat ook de corrosiesnelheid veel groter is. Afb. 8 toont de waarschijnlijkheid waarmee spleetcorrosie optreedt als functie van de verhouding tussen het oppervlak buiten de spleet en het spleetoppervlak. Opmerkelijk is, dat wat rvs AISI 304 betreft deze waarschijnlijkheid tot een verhouding 800/1 exponentieel toeneemt, terwijl de waarschijnlijkheid wat rvs AISI 316 en INCOLLOY ALLOY 825 betreft, na de verhouding 100/1 vrijwel constant blijft.
Kathodische bescherming
Kathodische bescherming is een techniek waarmee de potentiaal van een te beschermen object verlaagd wordt, waardoor de corrosiesnelheid aanzienlijk afneemt. Dit kan bereikt worden door het object elektrisch geleidend te verbinden met een metaal met een lagere potentiaal (wat dan de anode wordt, welke versneld in oplossing gaat), of door het object elektrisch een lagere potentiaal op te dringen. Deze beschermingsmethode is in het algemeen niet geschikt voor roestvast staal of andere passieve legeringen omdat hierdoor de functie van het beschermende oxidelaagje verdwijnt. Toch kan kathodische bescherming van rvs zin hebben als in een bepaalde constructie spleetcorrosie verwacht wordt [4]. Deze methode is echter alleen geschikt voor austenitische rvs-soorten omdat bij ferritische, martensitische en precipitatiehardende rvs-soorten een aanzienlijk risico op waterstofbrosheid bestaat. Tijdens kathodische reacties komt in zure milieus immers waterstof vrij volgens de reactie 2H+ + 2e--> H2 [4].
Het risico van het ontstaan van waterstofbrosheid is bij ferritische en martensitische legeringen groter omdat deze brosser zijn dan austenitische legeringen.
Onderzoek is uitgevoerd om meer inzicht te krijgen in de maximale diepte van spleten welke kathodisch beschermd kunnen worden [5]. Hierbij is aangetoond dat tijdens kathodische bescherming de pH in de spleet aanzienlijk wordt verhoogd. Dit geeft aan dat de kathodische reacties in de spleet de overhand hebben. Afb. 9 toont de pH in de spleet als functie van de tijd, waarbij na 20 uur de kathodische bescherming is ingezet. Hoe dieper in de spleet, hoe minder het oppervlak beschermd wordt door de zinkanode, hetgeen uit de grafiek ook op te maken is (bij grotere diepte heerst een lagere pH).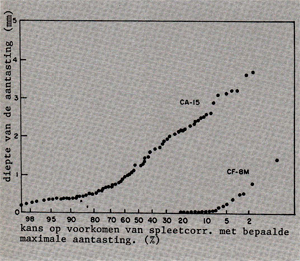
Afb. 7. Voorbeeld van een voor de spleetcorrosietest van Anderson typerende grafiek [2}.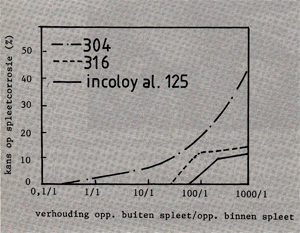
Afb. 8. Waarschijnlijkheid waarmee spleetcorrosie optreedt als functie van de verhouding tussen het oppervlak buiten de spleet en het spleetoppervlak, proefstukken zijn 30 dagen aan stromend zeewater blootgesteld [2}.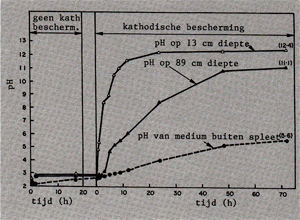
Afb. 9. De pH in de spleet als functie van de tijd, waarbij na 20 uur de kathodische bescherming is ingezet d.m.v. verbinding met zinkanode. Oplossing (aangezuurd): 0.6 M NaCl [5].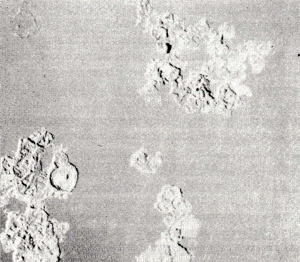
Afb. 10. Spleetcorrosie onder mosselaangroei op rvs AISI 304(foto: MCE).
Stroomsnelheid van het medium
Ook naar de invloed van de stroomsnelheid van het medium op spleetcorrosie is onderzoek uitgevoerd [6]. Hierbij is aangetoond dat snelstromend zeewater meer kans op spleetcorrosie geeft dan stilstaand zeewater. Dit effect wordt toegeschreven aan de snellere zuurstoftoevoer naar het kathodisch oppervlak bij stromend zeewater. Spleetcorrosie kan ook onder aangroei van b.v. zeepokken, mosselen of andere organismen plaatsvinden (zie afb. 10). In dergelijke gevallen is snelstromend water gunstig omdat dit soort organismen zich hier minder thuis voelen.
Samenvatting
Ter voorkoming van spleetcorrosie kunnen de volgende maatregelen genomen worden:
1. Vermijd spleten zoveel mogelijk
2. Geef gevoelige plaatsen (spleten) een bestendige coating
3. Verklein de verhouding kathode/anode door de kathodische oppervlakken van een isolerende coating te voorzien.
4. Gebruik een inhibiterende pasta in de spleet
Tot slot volgt nog een opmerking betreffende spleetcorrosie op lasfouten. Dit kan op twee manieren ontstaan:
1. T.g.v. onvoldoende doorlassing, waardoor aan de onderzijde van de lasverbinding een spleet ontstaat.
2. T.g.v. een geheel ontbrekendeen/of gebrekkige inbranding op de laskant, waardoor ter plaatse van de overgang lasmetaal/warmtebeïnvloede zone een spleet ontstaat.
Afb. 11 toont een voorbeeld van spleetcorrosie wat t.g.v. een gebrekkige inbranding is ontstaan, afb. 12 toont een doorsnede over deze las.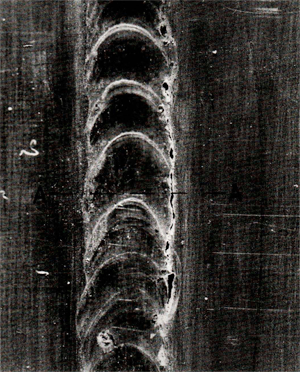
Afb. 11. Spleetcorrosie op de grens lasmetaal-warmtebeïnvloede zone. De spleet is t.g.v. slechte inbranding ontstaan (foto: MCE).
Afb. 12. Detail van doorsnede A-A, geëtst, vergroting 50x. Rechts is het lasmetaal, Links is de warmtebeïnvloede zone. De rafelige kanten zijn kenmerkend voor spleetcorrosie (foto: MCE).
Literatuuropgave:
1. L. Rosenfeld, localized corrosion, National Association of Corrosion Engineers, Houston, Tex., 1974, p 373.
2. D. B. Anderson, 'Statistica I Aspectsof Crevice Corrosion in Sea Water', 'Galvanic and Pitting Corrosion Field and Iabaratory Studies',
ASTM-STP576, American Society for Testing and Materials, 1976, p 231 .
3. O. B. Eli is and F.L. LaQue, Corrosion, Vol. 7, no. 11, p. 362.
4. T.P. May, H.A. Humble, Corrosion Vol. 8, no. 2, p. 50.
5. T.J . Lennoxand M.H. Peterson, NRL-Report2374, Naval Research Laboratory, Washington DC.
6. M.H. Peterson, T.J. Lennox, Mater, Prot., p. 23, january 1970.
7. B.E. Wilde, Localized Corrosion, National Association of Corrosion Engineers, Houston, Texas, p. 342, 1974.



