Corrosie van Roestvast staal Deel 2
Zoals de naam al doet vermoeden; putcorrosie is een vorm van lokale aantasting, welke het ontstaan van putjes in het oppervlak tot gevolg heeft. Deze corrosievorm is vooral gevaarlijk als de putten het metaal perforeren. Uit economisch oogpunt wordt vorming van brede ondiepe putten in sommige gevallen aanvaard.
Putcorrosie
Putcorrosie, waarvan afb. 1 een voorbeeld toont, ontstaat t.g .v. heterogeniteiten aan het oppervlak. Hetzij aan de metaalzijde, hetzij aan de milieuzijde. Wat het eerste geval betreft, kunnen insluitseis als bv. sulfiden de oorzaak van het ontstaan van een put zijn, volgens het mechanisme achter galvanische corrosie, zal het minst edele deel (hetzij het insluitsel hetzij de onmiddellijke omgeving van het insluitsel) in oplossing gaan. Een heterogeniteit aan de milieuzijde van het oppervlak kan b.v. een luchtbel of een zoutdruppel zijn.
Bij het ontstaan van putcorrosie in passieve metalen als rvs wordt aangenomen, dat het passieve oxidehuidje plaatselijk verzwakt is door onregelmatigheden in het onderliggende metaal (b .v. insluitsels, precipitaten of opeenhoping van roosterfouten). Aldaar kunnen agressieve ionen zoals chloride-ionen aan het oppervlak worden geadsorbeerd waardoor ter plaatse het elektrisch veld zal veranderen.
Voor het ontstaan van de putten moet een kritische grenspotentiaal, de zgn. doorbraak- of kritische pittingpotentiaal, overschreden worden.
Het elektrisch veld over de zwakke plaatsen in het oxidehuidje wordt dan dermate hoog, dat b.v. chloride-ionen in het oppervlak kunnen penetreren, waardoor microputjes worden gevormd. In sommige gevallen zullen deze putjes weer repassiveren (opnieuw een beschermend oxidelaagje vormen). In geval van een ernstige verstoring van het oppervlak of als de repassiveringssnelheid te laag is, zal het microputje zich uitbreiden tot een grotere put, waardoor het mechanisme wordt versneld. Deze versnelling wordt veroorzaakt doordat de gevormde positieve metaalionen het elektrisch evenwicht verstoren . Ter herstel van dit evenwicht zullen negatieve ionen naar de put migreren (zie afb. 2).
Afb. 1. Ernstige aantasting t.g.v. putcorrosie van rvs AISI 316Ti warmtewisselaarpijpen. (foto: MCE, Leiden)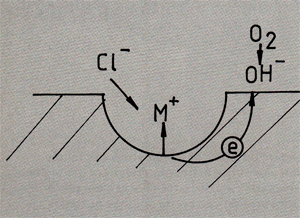
Afb. 2. Principeschets van het mechanisme van putcorrosie nadat de initiatie heeft plaatsgevonden. Door het ontstaan van positieve M+ -ionen worden negatieve ionen als Cl- -Cl- -ionen aangetrokken waardoor het proces versneld wordt. 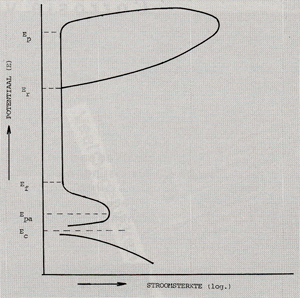
Afb. 3. Polarisatiekromme van een passief metaal. Ep = pittingpotentiaal, Er= repassiveringspotentiaal, Ef = flade potentiaal, Epa = passiveringspotentiaal, Ec = corrosiepotentiaal.
Potentiostaatmetingen
Een indicatie van het putcorrosiegedrag van een metaal kan verkregen worden aan de hand van polarisatiemetingen m.b.v. een potentiostaat (zie deel1 van deze serie). Afb. 31aat de polarisatiekromme van een passief systeem zien. Begonnen is een kathodische stroom door het metaal te sturen, de kathodische kromme is in principe gelijk aan die van koolstofstaaL Na het passeren van de corrosiepotentiaal, waar het anodische gedeelte van de grafiek begint, is het verloop aanvankelijk nog gelijk aan dat van koolstofstaal, hier begint het metaal te oxideren.
Echter spoedig zal de stroomsterkte terug gaan lopen, de potentiaal waarbij dit gebeurt wordt passiveringspotentiaal genoemd. Hier vormt zich t.g.v. de anodische reacties een afsluitend oxidelaagje op het oppervlak, de stroom loopt terug tot ze vrijwel de nulwaarde bereikt heeft (dit punt wordt de fladepotentiaal genoemd) en zal tijdens het verder opvoeren van de potentiaal deze waarde behouden.
Tot op een gegeven moment de pittingpotentiaal bereikt wordt waarbij microputjes ontstaan, welke t.g.v. het verder opvoeren van de potentiaal spoedig uitgroeien tot grote putten. Omdat de potentiaal opgevoerd wordt, en omdat het aantal en de afmeting van de putten steeds groter wordt, zal de stroomsterkte ( = corrosiesnelheid ) snel oplopen. Om de kromme af te maken, moet het potentiaalverloop op een gegeven moment omgedraaid worden. Aanvankelijk zal de stroomsterkte op blijven lopen, maar t.g.v. de dalende potentiaal komt hierin een keerpunt. De potentiaal waarbij de stroomsterkte weer dezelfde waarde bereikt heeft als voor de putvorming, wordt de repassiveringspotentiaal genoemd. Deze is een maat voor het herstellend vermogen van het metaal. Met enig voorbehoud kan gesteld worden dat een hogere pitting-en repassiveringspotentiaal van het betreffende metaal in het betreffende milieu een hogere weerstand tegen putcorrosie en een beter herstellend vermogen aanduiden. Bij interpretatie van de gegevens moet echter ook rekening worden gehouden met de zgn. redoxpotentiaal. De redoxpotentiaal geeft de evenwichtspotentiaal aan van in een bepaald milieu verlopende redoxkoppels, de anodische reactie is hierbij dus niet het oplossen van het eerroderende metaal (zoals bij de corrosiepotentiaal) maar één of meer anodische reacties van bestanddelen afkomstig uit het milieu.
Vandaar dat de redoxpotentiaal bepaald wordt door de potentiaal tussen inerte elektrode (platina elektrode) en een referentie-elektrode te meten. De redoxpotentiaal is kenmerkend voor een bepaald milieu.
Zo kan de redoxpotentiaal worden verlaagd door de H+ -concentratie te verlagen of de OH- -concentratie te verhogen. M.a.w., een verhoging van de pH levert een daling van de redoxpotentiaal op.
Nu is het zo dat in geval de redoxpotentiaal positiever is dan de pittingpotentiaal, er putcorrosie op zal treden. Ligt de redoxpotentiaal ver genoeg onder de pittingpotentiaal, dan zal er geen putcorrosie optreden. Vandaar dat het wenselijk is naast de pittingen repassiveringspotentiaal van het metaal in het betreffende milieu tevens inzicht te hebben in de redoxpotentiaal van het milieu. Bij een bereikt elektrochemisch evenwicht (d.w.z. dat het milieu verzadigd is van ijzeren andere metaalionen, dit kan in een gesloten systeem voorkomen), is de redoxpotentiaal gelijk aan de corrosiepotentiaaL Is het evenwicht niet bereikt, dan ligt de redoxpotentiaal iets boven de corrosiepotentiaal.
Het zal duidelijk zijn dat potentiestaatmetingen slechts een indicatie zijn, en dat ze geen sluitende conclusie betreffende het putcorrosiegedrag van een bepaald metaal in een bepaald milieu geven.
Een potentiostaatmeting is immers een simulatieproces waarbij vooral de factor tijd niet overeenkomt met de werkelijkheid . De pittingpotentiaal wordt tijdens de proef beïnvloed door de snelheid waarmee de potentiaal opgevoerd wordt, de zgn. scansnelheid. Hoe lager deze snelheid, hoe meer het systeem de kans krijgt zich op de nieuwe situatie in te stellen. Omdat een potentiostaatmeting dus niet te hoog moet zijn is een vaak toegepaste scansnelheid 20 mV / min. Ook moeten tijdens de proef de praktijkomstandigheden zoals spanningen in het metaal, de oppervlaktegesteldheid, een bewegend medium (roeren) etc. zoveel mogelijk benaderd worden.
Voorbeeld
Voor een bepaald milieu moet een materiaalkeuze worden gedaan. Er kan worden gekozen tussen b.v. rvs AISI 304 en 316. Bekend is dat de putcorrosiebestendigheid van AISI 316 veel beter is dan die van AISI 304, de prijs van AISI 316 is echter hoger. Als nu blijkt dat de redoxpotentiaal van het betreffende milieu negatiever is dan de pittingpotentiaal van het AISI 304 in het betreffende milieu, dan is het niet nodig om het duurdere AISI 316 toe te passen. Als ook de repassiveringspotentiaal boven de redoxpotentiaal ligt, dan wordt op safe gespeeld. Ligt de redoxpotentiaal in de buurt van of boven de pittingpotentiaal, dan moet voor AISI 316 worden gekozen. Tabel1 laat de redoxpotentiaal van leidingwater en de pitting-en repassiveringspotentiaalvan AISI 304 en 316 in dit milieu zien. Uit deze tabel kan opgemaakt worden dat zowel AISI 304 als AISI 316 tegen leidingwater zijn opgewassen.
Anders ligt dit bij een milieu als geconcentreerde pekel op hogere temperatuur. Hiertegen bl ijkt zelfs AISI 316 niet bestand te zijn. Tabel2 toont enkele meetresultaten waaruit duidelijk blijkt dat de redoxpotentiaal ver boven de pittingpotentiaalligt. Bijvoorbeeld in geval van opslag van chloridehoudende oplossingen in een rvs-tank, kan overwogen worden de pH van de oplossing te verhogen door er b.v. natriumhydroxide aan toe te voegen . Uit tabel2 blijkt dat de redoxpotentiaal door deze pH verhoging tot onder pittingpotentiaal daalt, waardoor de kans op het optreden van putcorrosie aanzienlijk kleiner geworden is. 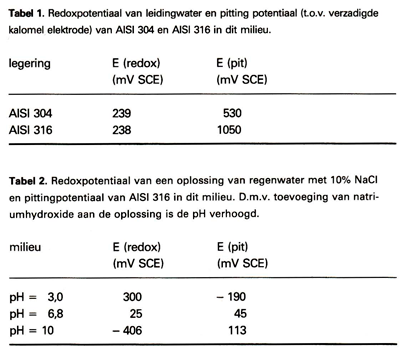
IJzerchloride-test (ASTM-practice G47-76)
Niet alle informatie betreffende het putcorrosiegedrag hoeft langs elektrochemische weg verkregen te worden . De ijzerchloridetest is een dompeltest welke informatie geeft over de vorm, afmeting en verdeling van de putten over het oppervlak. Voor deze test is een oplossing nodig van 100 gram ijzerchloride (FeCI3. 6H2O) in 900 ml gedestilleerd water, waardoor een oplossing met 6 gew% ijzerchloride verkregen wordt.
Afhankelijk van de gewenste agressiviteit (welke ook de tijdsduur van de proef bepaalt) wordt voor een temperatuur tussen de 22°C en 50°C gekozen . Evaluatie vindt plaats door het gewichtsverlies te meten en d.m.v. visuele inspectie, welke informatiegeeft over de vorm, verdeling en afmetingen van de putten (afb. 4 en afb. 5). Soms wordt ter verhoging van de agressiviteit aan de oplossing nog wat zoutzuur toegevoegd. Putten welke in chloridehoudende milieus ontstaan, kenmerken zich door hun klokvormige uiterlijk.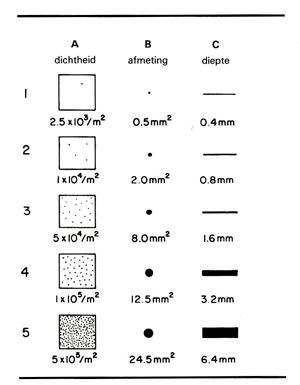
Afb. 4. Standaard vergelijkingstabel voor putten volgens ASTM Practice G46-76.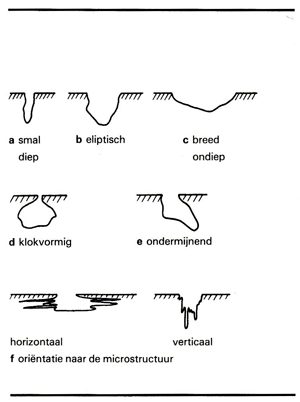
Afb. 5. Verschillende vormen waarop een put zich kan uitbreiden.
Invloed van de legeringselementen op de pittingbestendigheid
De twee meest voorkomende legeringselementen in roestvast staal (chroom en nikkel) verhogen naast de weerstand tegen algemene corrosie ook de weerstand tegen putcorrosie, zoals afb. 6 en afb. 7 duidelijk maken. De potentialen bij de afbeeldingen zijn t.o.v. een verzadigde calomel elektrode gegeven (SCE = Saturated Calomel Electrode). Vooral tussen de 25% en 35% chroom blijkt een weinig extra chroomtoevoeging grote invloed te hebben op de pittingpotentiaal. De invloed van nikkel op de pittingpotentiaal verloopt meer lineair.
De belangrijkste reden waarom molybdeen aan roestvast staal wordt toegevoegd (zoals bv. rvs AISI 316 en 317) is het feit dat dit element de putcorrosiebestendigheid in chloridehoudende milieus aanzienlijk verhoogt. Afb. 8 onderstreept dit. Naast bovengenoemde elementen hebben ook stikstof, silicium en vanadium een gunstige invloed. In de matrix opgeloste koolstof heeft geen invloed maar uitgescheiden carbiden beïnvloeden de putcorrosiebestendigheid negatief.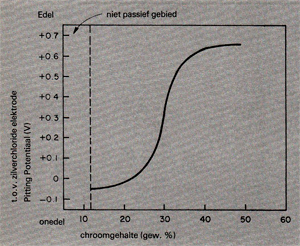
Afb. 6. Invloed van het chroomgehalte op de pitringpotentiaal van ijzer-chroom legeringen in een niet beluchte 0, 1 N NaCl oplossing bij 25°C. Alle potentialen in deze afbeeldingen zijn t.o.v. een verzadigde kalomel referentie elektrode. [3]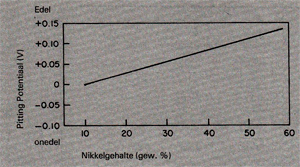
Afb. 7. Invloed van het nikkelgehalte op de pitringpotentiaal van Fe-15%Cr legeringen in een niet beluchte 0, 1 N NaCl oplossing bij 25°C. [3}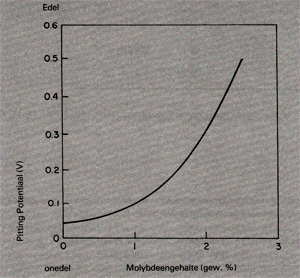
Afb. 8. Invloed van het molybdeengehalte op de pittingpotentiaal van Fe-15%Cr-13%Ni legeringen in een niet beluchte 0, 1 N NaCl oplossing bij 25°C. [3]
Invloed van de microstructuur
De microstructuur kan een grote invloed op de putcorrosiegevoeligheid van rvs hebben. Heterogeniteiten als sulfiden, delta ferriet, sigma fase, precipitaten in precipitatiehardbare rvs-soorten, uitscheidingen op korrelgrenzen enz. beïnvloeden allen de putcorrosiebestendigheid.
Onderzoek heeft aangetoond, dat het chroomgehalte in de sulfideinsluitseis een grote invloed heeft op de vorming van putten op deze insluitseis [1). Omdat mangaan een grotere affiniteit tot zwavel heeft dan chroom, wordt het chroomgehalte van de insluitseis mede bepaald door het mangaangehalte van de legering (afb. 9). een hoger mangaangehalte betekent een lager chroomgehaltevan de insluitsels, wat inhoudt, dat de pittingpotentiaal daalt (afb. 10). De aanwezigheid van deltaferriet en sigmafase wordt wat de putcorrosiebestendigheid betreft als ongunstig beschouwd. Over het algemeen zijn de precipitatiehardende rvs-soorten gevoeliger voor putcorrosie dan de austenitische. Dit komt door de aanwezigheid van uitscheidingen en precipitaten, welke geschikte initiatieplaatsen voor putcorrosie zijn.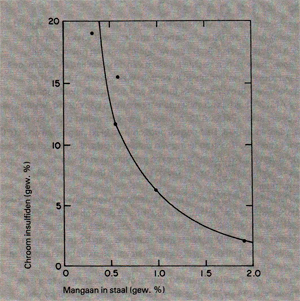
Afb. 9. Chroomgehalte van sulfide-uitscheidingen in een Fe-13%Cr-0,3%S legering als functie van het mangaangehalte van deze legering. [4]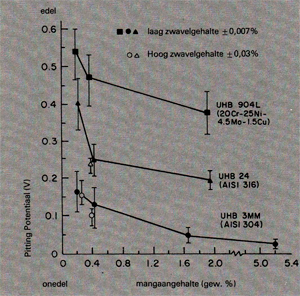
Afb. 10. Invloed van het mangaangehalte op de pittingpotentiaal van enkele rvs-soorten in een 3%NaCI oplossing. [5]
Invloed van het milieu
De meeste schade t.g.v. putcorrosie is te wijten aan de aanwezigheid van chlorideionen. Wat rvs in hoog chloridehoudende milieus betreft, zijn eigenlijk alleen legeringen als AISI 316, AIS I317 en Hastelloy Alloy G min of meer bestand tegen putcorrosie.
Wat de andere halogeenionen betreft, geeft ook bromide aanleiding tot pitting, fluoride en jodide oplossingen blijken minder agressief te zijn . Negatieve ionen welke de neiging tot pitting verlagen, zijn SO42-, OH-, CIO3-, CrO42- en NO3- [2]. Hun min of meer inhibiterende werking is afhankelijk van de concentratie en de verdere samenstelling van het milieu. Verlagen van de pH-waarde blijkt vrijwel geen invloed op de pittingpotentiaal te hebben (afb. 11 ). Dit wordt toegeschreven aan het feit dat de pH-waarde in de put grotendeels door de corrosiereactie zelf wordt bepaald, extra toevoer van H+-ionen van buitenaf heeft hierop weinig invloed. Zoals al vermeld, blijkt de pH-waarde wel grote invloed op de redoxpotentiaal te hebben.
Verhoging van de temperatuur verlaagt de energie welke toegevoerd moet worden voor het laten plaatsvinden van een reactie, zo ook in dit geval. Afb. 12 laat zien dat verhoging van de temperatuur de putcorrosiebestendigheid verlaagt. Opmerkelijk is, dat deze wat rvs AISI 316 betreft op een gegeven moment constant blijft.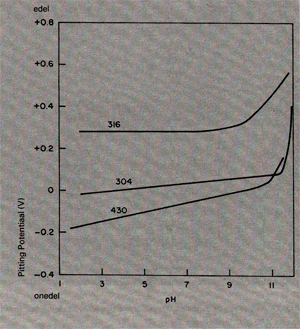
Afb. 11. Invloed van de pH op de pittingpotentiaal van verschillende rvs-soorten in een 3%NaCI-oplossing. [6]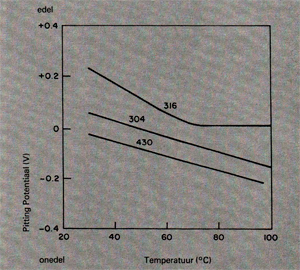
Afb. 12. Invloed van de temperatuur op de pittingpotentiaal van verschillende rvs-soorten op een 3%NaCI oplossing. [6]
Invloed van de oppervlaktegesteldheid
De rol welke de oppervlaktegesteldheid op de corrosiebestendigheid (dus ook putcorrosiebestendigheid) speelt, wordt vaak onderschat. Toch is deze aanzienlijk. De aanwezigheid van een ruw oppervlak, krassen, butsen, een slechte kwaliteit van de oxidelaag etc. beïnvloeden de putcorrosiebestendigheid in negatieve zin. In afb. 13 wordt de kwaliteit van de oxidehuid als functie van de putdichtheid gegeven. Rvs AlSI 304L is bij verschillende temperaturen geoxideerd, waarna het enige tijd in een FeCI3. AICl3 oplossing met een weinig LiCi toevoeging is ondergedompeld. De hoogste putdichtheid blijkt na gloeien op 300°C voor te komen. De verandering van putdichtheid welke in deze grafiek is weergegeven, wordt toegeschreven aan verandering van de geleidbaarheid van de oxidehuid na gloeien op de verschillende temperaturen.
Een lasbehandeling zal altijd een plaatselijke kwaliteitsvermindering van de oxidehuid te zien geven, de praktijk heeft dan ook uitgewezen, dat putcorrosieproblemen vaak net naast of op de las voorkomen. Vandaar dat het altijd aanbevelenswaardig is, een las te beitsen en te passiveren, wat inhoudt, dat de kwaliteit van de oxidehuid ter plaatse aanzienlijk verbetert. Een mooi voorbeeld van putcorrosie op of net naast de las tonen de afbeeldingen 14. Deze vorm van aantasting had voorkomen kunnen worden door de las en warmtebeïnvloede zone te beitsen en passiveren.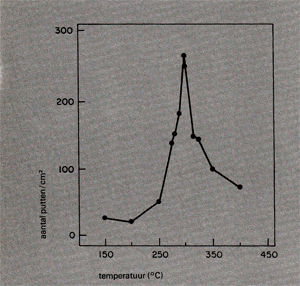
Afb. 13. Invloed van de oxidatietemperatuur in droge lucht op de putdichtheid van rvs AISI 304L loxidatietijd: 2 uur). [7]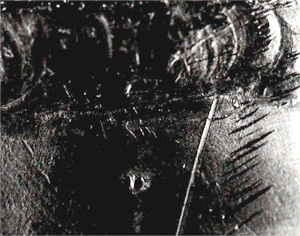
Afb. 14. Putcorrosie in de warmtebeïnvloede zone van een las. (foto: MCE, Leiden)
Literatuur
1. C.W. Kovach et al., Trans. ASM, Vol61, p. 575, 1968.
2. S. Szklarska-Smialowska, localized corrosion, National Association of Corrosion Engineers, Houston, Texas.
3. J. Horvath & H.H. Uhlig, J. Electrochem. Soc., Vol115, p. 791, 1968.
4. M. Henthorne, Sulfide inclusions in steel, ASM, Metals Park Ohio, p. 445, 1975.
5. J . Degerbeck & E. Word, Werkst. Korros. Vol25, p. 172, 1974.
6.Z. Szklarska-Smialowska & Janik Czachor, Corrosion Science Vol7, p.65, 1967.
7. G. Bianchi et al., Localized corrosion, NACE, Houston Texas, 1974, p. 399.



