Sulfidatie van Roestvast Staal
Zwavel is een van de meest voorkomende corrosieve verontreinigingen in industriële omgevingen waar hoge temperaturen heersen en komt direct op de tweede plaats na oxidatie in frequentie van optreden. Zwavel is in de regel aanwezig als verontreiniging in brandstoffen of toevoermateriaal. Het zijn met name stookoliën die zijn verontreinigd met zwavel, variërend van fracties van 1% tot ongeveer 3%. Steenkolen kunnen 0,5 tot 5% zwavel bevatten al naar gelang hun herkomst. Toevoermateriaal voor calcineringsprocessen in de procesindustrie is vaak verontreinigd met uiteenlopende hoeveelheden zwavel.
Door: A.J. Schornagel
Als er verbranding plaatsvindt met een overmaat lucht om volledige verbranding te garanderen van brandstof voor het opwekken van warmte in tal van industriële processen, zoals bij kolen- of oliegestookte energieopwekking, reageert zwavel in de brandstof met zuurstof tot zwaveldioxide (SO2) en zwaveltrioxide (SO3). Een atmosfeer van dit type is in het algemeen oxiderend. Oxiderende milieus zijn meestal veel minder corrosief dan reducerende milieus, waarin zwavel voorkomt in de vorm van waterstofsulfide (H2S). Sulfidatie in zowel oxiderende als reducerende milieus wordt vaak versneld door andere brandstofverontreinigingen, zoals natrium, kalium en chloor, die tijdens de verbranding met elkaar kunnen reageren en met zwavel onder vorming van metaalzoutdampen. Deze zoutdampen kunnen tijdens afkoeling neerslaan op het metaaloppervlak, hetgeen resulteert in versnelde sulfidatie aantasting. Oxiderende milieus die hoge concentraties SO2 bevatten kunnen ontstaan tijdens het chemische proces dat wordt gebruikt voor de fabricage van zwavelzuur. In dit geval wordt zwavel gebruikt als toevoermateriaal. Verbranding van zwavel met overmaat lucht vindt plaats in een zwaveloven bij ongeveer 1150 tot 1200°C. Het geproduceerde gas bevat zo’n 10 tot 15% SO2 tezamen met 5 tot 10% O2 (rest N2) dat dan wordt omgezet in SO3 voor zwavelzuur.
In veel industriële processen vindt verbranding plaats onder stoechiometrische of substoechiometrische omstandigheden teneinde toevoermateriaal om te zetten in procesgassen bestaande uit H2, CO, methaan (CH4) en andere koolwaterstoffen. Zwavel wordt omgezet tot H2S. Het milieu is in dit geval reducerend en wordt gekenmerkt door lage zuurstofpotentialen. Kolenvergassing is een gangbaar voorbeeld van een proces waarbij dit soort atmosfeer wordt opgewekt. Reducerende condities kunnen ook overheersen op lokale plaatsen. Voorts kan neergeslagen as op het metaaloppervlak soms een oxiderend milieu doen overgaan in een reducerend milieu onder de neerslag. In de meeste gevallen ontlenen metalen en legeringen hun weerstand tegen sulfidatie aan de aanwezigheid van een beschermende oxidelaag. De meeste legeringen voor gebruik bij hoge temperatuur vormen een chroomoxidelaag. In oxiderende milieus ontstaan oxidelagen veel makkelijker wegens de hoge zuurstofactiviteit. Oxidatie zal dan de corrosiereactie domineren. Als er sprake is van een reducerend milieu (lage zuurstofpotentialen), dan ontstaat er een strijd tussen oxidatie en sulfidatie. Verlaging van de zuurstofpotentiaal maakt dat het milieu sterker sulfiderend wordt, waardoor de sulfidatie gaat overheersen. Verhoging van de zuurstofpotentiaal resulteert doorgaans in een minder sulfiderend milieu met dominerende oxidatie. Sulfidatie wordt dus zowel gecontroleerd door zwavel- als door zuurstofactiviteit. Als corrosie uit meer dan een modus bestaat, waaronder sulfidatie, dan bepaalt sulfidatie in het algemeen de materiaalselectie.
Sulfidatieweerstand van roestvast staal
Net als bij oxidatie, hangt de weerstand tegen sulfidatie samen met het chroomgehalte. Ongelegeerd ijzer zal vrij snel worden omgezet in ijzersulfidescale, maar als ijzer wordt gelegeerd met chroom, dan neemt de sulfidatieweerstand toe, zie afbeelding 1. Silicium biedt eveneens enige bescherming tegen sulfidatie.
Het nikkel/nikkelsulfide eutecticum met laag smeltpunt, kan ontstaan op roestvast staal dat meer dan 25% Ni bevat, zelfs in de aanwezigheid van een hoog chroomgehalte. Het optreden van gesmolten fazen tijdens gebruik bij hoge temperatuur kan leiden tot catastrofale vernietiging van de legering. Behalve van de gebruikelijke factoren tijd, temperatuur en concentratie hangt sulfidatie af van de vorm waarin het zwavel voorkomt. Van bijzondere interesse zijn de effecten van zwaveldioxide, zwaveldamp, waterstofsulfide en rookgassen.
Reactie met zwaveldioxide
Roestvast staal dat meer dan 18 tot 20% Cr bevat is bestand tegen droge zwaveldioxide. Bij 24 uur proeven over een temperatuurstraject van 590 tot 870°C, werd er alleen een verkleuring waargenomen bij type 316 in atmosferen variërend van 100% O2 tot 100% SO2. De corrosiesnelheid van type 316 in SO2-O2-N2 atmosferen bedroeg 0,12 mm/jaar (4,9 mils/year) bij 640 tot 655°C. Fe-15Cr (typen 430, 440), Fe-30Cr (ongeveer type 446) en Fe-18Cr-8Ni (type 304) vertoonden in de weergegeven volgorde toenemende weerstand tegen zwaveldioxide.
Reactie met zwaveldamp
Zwaveldamp tast austenitisch roestvast staal vlot aan. Tijdens proeven werden de in tabel 1 weergegeven corrosiesnelheden gemeten in stromende zwaveldamp bij een temperatuur van 570°C. In vloeibare zwavel zijn de meeste austenitische typen bestand tot 200°C, waarbij de gestabiliseerde typen 321 en 347 bevredigende prestaties vertonen tijdens bedrijf bij temperaturen tot 445°C.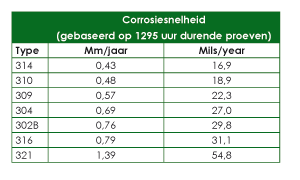
Tabel 1. Corrosiesnelheid van een aantal roestvast-staaltypen in stromende zwaveldamp.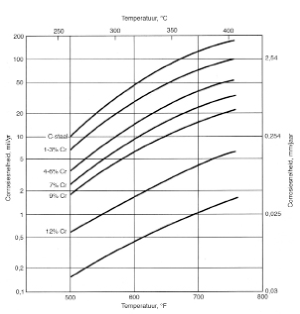
Afbeelding 1. Effect van het chroomgehalte op de weerstand tegen sulfidatie van ijzerlegeringen in een waterstofvrij milieu.
Reactie met waterstofsulfide
De corrosiesnelheid in waterstofsulfide hangt af van de concentratie, temperatuur, druk en doorlaatbaarheid van de sulfidescale. De aanwezigheid van chroom in het staal helpt bij het stabiliseren van de scale en het vertragen van de diffusie. Als echter waterstof aanwezig is bij hoge druk en temperatuur dan is de aantasting heftiger, zelfs in die mate dat laag-chroomhoudend staal niet meer voldoet. Waterstof-waterstofsulfide (H2-H2S) mengsels zijn kenmerkend voor de gastroom in katalytische reformatoreenheden. Katalytisch reformeren wordt toegepast in olieraffinaderijen voor het opwaarderen van het octaangetal van benzine. Er is bij katalytisch reformeren een grote hoeveelheid waterstof aanwezig en zwavel in de naftacharge reageert met waterstof tot waterstofsulfide. Er is ernstige corrosieve aantasting aangetroffen bij procesapparatuur als gevolg van waterstofsulfide in tal van katalytische reformatoren en ontzwavelingseenheden.
Er is corrosie als gevolg van waterstofsulfide gemeld bij verscheidene raffinagebewerkingen uitgevoerd in het laboratorium, bij proeven in proeffabrieken, bij proeven te velde en in commerciële apparatuur. Austenitisch roestvast staal (18Cr-8Ni) bleek het best bestand, gevolgd door alleen chroomhoudend roestvast staal (12 tot 16% Cr). Laag-chroomhoudend staal (0 tot 9% Cr) werd het sterkst aangetast. Het is interessant om op te merken dat een bescheiden hoeveelheid nikkel, toegevoegd aan ijzer-chroomlegeringen, de weerstand van die legeringen tegen sulfidatie in H2-H2S milieus significant verhoogt, afbeelding 2. Sulfidatie van legeringen in H2-H2S mengsels wordt beschreven door het isocorrosie diagram dat de corrosiesnelheid toont als functie van de H2S concentratie en temperatuur. Het isocorrosie diagram van afbeelding 3 toont de invloed van waterstofsulfide en temperatuur op de weerstand tegen sulfidatie van austenitisch roestvast staal.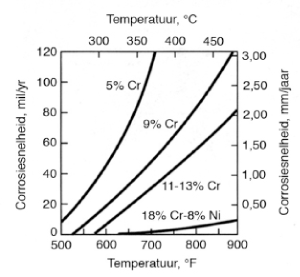
Afbeelding 2. Corrosiesnelheden van Fe-Cr en Fe-Cr-Ni legeringen in H2-H2S milieus (H2S concentraties hoger dan 1mol%).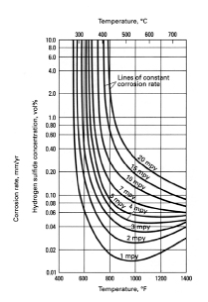
Afbeelding 3. Isocorrosie diagram dat het effect toont van waterstofsulfide concentratie op de corrosiesnelheid (in mils/year) van austenitisch roestvast staal in waterstof atmosferen bij 1200 tot 3450 kPa. Expositietijd was langer dan 150 uur.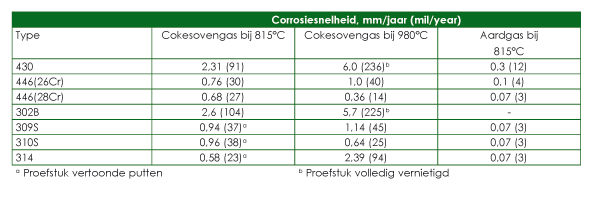
Tabel 2. Corrosiesnelheden van roestvast staal na expositie gedurende 3 maanden in rookgassen.
Invloed van zwavel in rookgassen en procesgassen
Het is buitengewoon moeilijk om corrosiesnelheden in rookgassen en procesgassen te generaliseren, omdat de gassamenstelling en temperatuur in een en dezelfde proceseenheid sterk uiteen kunnen lopen. Verbrandingsgassen bevatten gewoonlijk zwavelverbindingen. Zwaveldioxide is aanwezig als een oxiderend gas tezamen met kooldioxide, stikstof, koolmonoxide en overmaat zuurstof. Beschermende oxiden worden wel gevormd en afhankelijk van de exacte condities kan de corrosiesnelheid bij benadering dezelfde zijn als in lucht of iets groter. De weerstand van roestvast staal tegen normale verbrandingsgassen wordt vergroot door opeenvolgende verhogingen van het chroomgehalte, zie afbeelding 4. Tabel 2 toont het gunstige effect van chroom en de invloed van de brandstofbron. Reducerende rookgassen bevatten uiteenlopende hoeveelheden waterstofsulfide, waterstof, koolmonoxide, kooldioxide en stikstof. De corrosiesnelheden die in dit soort milieus worden aangetroffen zijn gevoelig voor het gehalte waterstofsulfide en de temperatuur. Te gebruiken materiaal dient eerst onder gebruiksomstandigheden te worden getest. Tabel 3 illustreert het effect van het zwavelgehalte op de corrosie van typen 309, 310 en 330 in oxiderende en reducerende rookgassen. Het schadelijke effect van hoge nikkelgehaltes is overduidelijk. 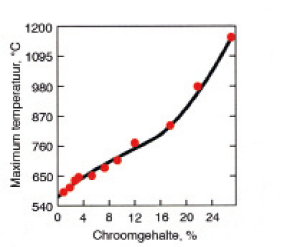
Afbeelding 4. Effect van chroom op de maximum oxidatieweerstand voor ijzer-chroom legeringen in een normale verbrandingsatmosfeer.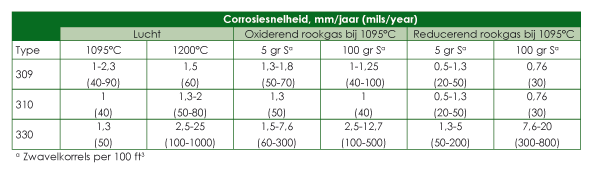
Tabel 3. Corrosiesnelheden van roestvast gietstaal in lucht en in oxiderende en in reducerende rookgassen.



