Lokale corrosievormen: putcorrosie: Deel 3: Invloed van de samenstelling van het milieu
Deel 3
Of onder praktijkomstandigheden in een gegeven milieu aan een gegeven stuk roestvast staal al dan niet putcorrosie zal optreden is afhankelijk van: de putpotentiaal en het oxiderend vermogen van de oplossing.
Putpotentiaal
De putpotentiaal is de potentiaal waarbij de passiviteit van het roestvaststaaloppervlak plaatselijk wordt doorbroken. De putpotentiaal kan voor een bepaalde metaal-milieucombinatie worden afgelezen uit een polarisatiecurve die is bepaald in het betreffende milieu met een proefstrip van het betreffende roestvast staal. Afbeelding 3 toont de polarisatiecurve van AISI 304 in een chloridehoudend milieu dat is aangezuurd met zwavelzuur. De ligging van de putpotentiaal is een maat voor de weerstand die het roestvast staal biedt tegen putcorrosie. Een hoger gehalte chloride of chloorhoudende verbindingen verplaatst de putpotentiaal naar een negatievere waarde. Verhogen van het chloridegehalte van een oplossing brengt dus een verhoogde kans op putcorrosie zich mee. Hierbij moet worden opgemerkt dat het verhogen van het chloridegehalte van 50 mg/l tot 500 mg/l doorgaans een groter risico met zich mee brengt dan een stijging van 20.000 mg/l tot 30.000 mg/l, alhoewel de absolute stijging in het chloridegehalte in het tweede geval veel hoger is. Dit is ongeveer te vergelijken met de kans op een lekke band bij het fietsen over een pad waar eerst een punaise lag en verderop 10 of de kans op een lekke band bij het fietsen door eerst honderd en later tweehonderd punaises. Honderd of tweehonderd maakt weinig uit. Je banden zijn in beide gevallen volledig geperforeerd. Ionen die een verschuiving van de putpotentiaal in de positieve richting veroorzaken zijn: SO4 2-, OH-, ClO3-, CO3 2-, Cr2O4
2- en NO3-. De grootte van het effect op de putpotentiaal is afhankelijk van hun concentratie en van de chlorideconcentratie in de oplossing. In zeer geringe concentraties kunnen bovengenoemde ionen ook een verlaging van de putpotentiaal veroorzaken. Het inhibiterende effect van de OH--concentratie is voor een drietal roestvaststaaltypen gegeven op afbeelding 4. Pas bij pH-waarden van circa 9 tot 11 blijken de putpotentialen een sterke toename in positieve waarde te vertonen.
Oxiderend vermogen
In het traject van pH 1,5 tot circa pH 9 à 10 heeft de pH-waarde weinig invloed op de putpotentiaal. In de praktijk blijkt echter dat in milieus met een lage pH-waarde er wel degelijk bij een gelijk chloridegehalte eerder putcorrosie zal optreden. Dit laat zich verklaren aan de hand van de tweede invloedsfactor, namelijk het oxiderend vermogen van de oplossing. Bij een lagere pH-waarde zijn er meer H+-ionen in de oplossing waardoor het oxiderend vermogen groter is. Natriumhypochloriet (ontsmettingsmiddel) is een goed voorbeeld van een stof die putcorrosie veroorzaakt door zijn sterk oxiderende vermogen en de gelijktijdige aanwezigheid van chloride en chloorhoudende verbindingen. Andere bekende stoffen die het oxiderend vermogen van een oplossing vergroten zijn Cu2+- en Fe3+-ionen en zuurstof en NO3--ionen. Zuurstof en NO3--ionen zijn behalve op het oxiderend vermogen ook van invloed op de vorming van de passieve laag op het roestvast staal en zijn hiermee dus ook van belang voor de putpotentiaal.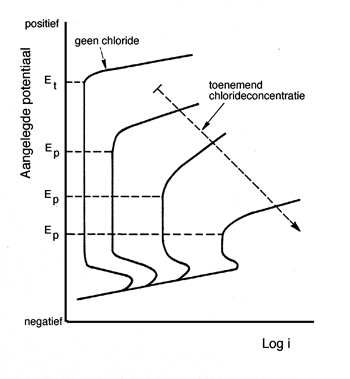
Afbeelding 3 V oor roestvast staal kenmerkende polarisatiecurven in een zwavelzuuroplossing bij een variërend chloridegehalte. Ep = putpotentiaal; Et = potentiaal waarbij transpassief gedrag optreedt.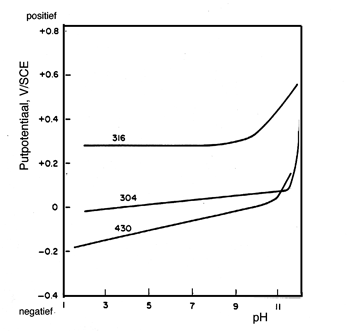
Afbeelding 4 H et effect van de pH-waarde op de putpotentiaal van verschillende roestvaststaaltypen in een 3 gew.% NaCloplossing.
Redoxpotentiaal en oxiderend vermogen
Het oxiderend vermogen van een oplossing komt tot uitdrukking in de redoxpotentiaal. De redoxpotentiaal is de potentiaal die wordt gemeten tussen een inerte elektrode, meestal platina en een referentie- elektrode. Doordat platina zich inert gedraagt en niet meedoet aan de reacties zullen de evenwichten van reductie- en oxidatiereacties (redoxreacties) van bestanddelen van de oplossing de uiteindelijke potentiaal bepalen die de platina elektrode aanneemt. Hoe positiever de redoxpotentiaal, hoe groter het oxiderend vermogen en hoe meer kans op het daadwerkelijk optreden van putcorrosie. Door verlaging van de pH neemt de redoxpotentiaal een positievere waarde aan. Ook door de verhoging van de concentratie Cu2+- en Fe3+-ionen neemt de redoxpotentiaal een posievere waarde aan. Of er in de praktijk daadwerkelijk putcorrosie zal optreden is afhankelijk van de ligging van de putpotentiaal ten opzichte van de redoxpotentiaal. Is de putpotentiaal duidelijk positiever, dan de redoxpotentiaal dan zal het roestvaststaaltype in het betreffende milieu niet onderhevig zijn aan putcorrosie. In het geval de redoxpotentiaal positiever is dan de in hetzelfde milieu gemeten putpotentiaal, dan doet zich wel putcorrosie voor. In het geval er een elektrochemisch evenwicht is bereikt (het milieu
is verzadigd met ijzer- en andere metaalionen), is de redoxpotentiaal gelijk aan de corrosiepotentiaal. Dit kan zich voordoen in gesloten systemen. Wordt geen evenwicht bereikt, bijvoorbeeld omdat er steeds een vers medium langsstroomt, dan is de redoxpotentiaal wat positiever dan de corrosiepotentiaal.
Temperatuur
De temperatuur heeft een sterke invloed op de ligging van de putpotentiaal. Afbeelding 5 toont voor drie gangbare roestvaststaal typen de invloed van de temperatuur op de putpotentiaal in een 3 gew.% NaCl-oplossing. Er blijkt dat bij een verhoging van de temperatuur een verschuiving naar negatievere waarden optreedt. Het risico ten aanzien van putcorrosie neemt toe. Er blijkt ook dat de grootte van de invloed van de temperatuur afhankelijk is van het legeringstype.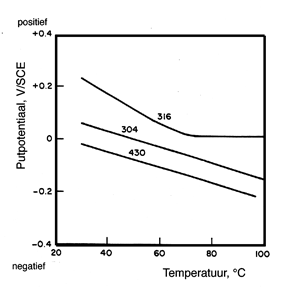
Afbeelding 5 H et effect van de temperatuur op de putpotentiaal van verschillende roestvast-staaltypen in een 3 gew. % NaCl-oplossing.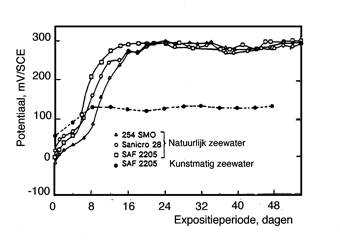
Afbeelding 6 H et verloop van de corrosiepotentiaal van roestvast staal in de tijd in natuurlijk zeewater en kunstmatig zeewater bij 8°C.
3.1 Microbiologische aspecten
Wanneer roestvast staal wordt blootgesteld aan natuurlijk zeewater dan is de corrosiepotentiaal aanvankelijk laag, maar deze neemt snel toe tot een bepaalde waarde. In kunstmatig, steriel zeewater (een 3% NaCl-oplossing) is een soortgelijke sterke potentiaaltoename niet waarneembaar. Afbeelding 6 toont dat de corrosiepotentiaal een waarde van 300 mV ten opzichte van SCEelektrode bereikt. Bovendien valt af te lezen dat de verandering in de corrosiepotentiaal onafhankelijk is van de legeringssamenstelling van de roestvaststaaltypen. Dezelfde potentiaaltoename is ook waargenomen bij andere passieve materialen, zoals titanium en NiCrMo-legeringen. Door de verhoging van de potentiaal die het roestvast staal aanneemt zal eerder putcorrosie optreden. Dit verschil in putcorrosiegedrag in natuurlijk en kunstmatig zeewater heeft verstrekkende gevolgen. Tot voor enige tijd werd de geschiktheid van een roestvaststaaltype bepaald in kunstmatig zeewater. Nu blijkt dat daarbij een belangrijk effect stelselmatig over het hoofd werd gezien met alle gevolgen van dien. Onderzoek heeft uitgewezen dat de potentiaaltoename het gevolg is van de vorming van een microbiologische slijmlaag op het metaaloppervlak. Deze zogenaamde biofilm die zich snel vormt op een inert oppervlak heeft een sterk katalytisch (bevorderend) effect op de kathodische reactie van het corrosieproces, te weten de zuurstofreductie (reactie 1). De anodische reactie blijkt niet te worden beïnvloed door de aanwezigheid van de biofilm. Het praktische gevolg van de hogere corrosiepotentiaal is een groter risico ten aanzien van de initiatie van put- en spleetcorrosie. De hogere kathodische stroomdichtheid veroorzaakt een snelle propagatie van zowel put- als spleetcorrosie. Natuurlijk zeewater is door de vorming van een biofilm aanzienlijk corrosiever dan kunstmatig zeewater. De vorming van een bioflim met bijkomende nadelige gevolgen kan ook optreden in brak water en in rivierwater. De activiteit van de biofilm is optimaal binnen een bepaald temperatuurtraject. In tropische wateren komen andere micro-organismen voor dan in de Noordzee waardoor ook het temperatuurtraject waarin de organismen actief zijn, zal verschillen. Verhoging of verlaging van de temperatuur tot buiten het optimale temperatuurtraject is van grote invloed op de activiteit van de biofilm en dus ook op het corrosiegedrag van roestvast staal in een dergelijk milieu. Als richtlijn kan worden aangehouden dat bij temperaturen boven 30 tot 40˚C het katalytische effect van de biofilm op de kathodische reactie niet meer optreedt. Een andere manier waarop micro-organismen van invloed kunnen zijn op het putcorrosiegedrag is door de vorming van agressieve stoffen. Er zijn bijvoorbeeld bacteriën die zwavelhoudende bestanddelen van het milieu omzetten in zwavelzuur. Hiertoe behoren de zogenaamde Sulfaat Reducerende Bacteriën (SRB). Hierbij ontstaan corrosieputten op plaatsen waar zich een kolonie bacteriën op het oppervlak bevindt. Vaak zijn lassen het doelwit omdat het ruwere oppervlak en eventuele porositeiten een goed houvast bieden voor de micro-organismen. De veelheid van soorten microorganismen en omstandigheden waaronder de verschilende soorten actief kunnen zijn laten we hier buiten beschouwing.
3.2 Stromingseffecten
De invloed van de stromingssnelheid op de initiatie van putcorrosie werd al eerder genoemd. De stabiliteit van beginnende putten in een stilstaand milieu is groter dan in een snelstromend milieu. In een zure ijzer(III)chlorideoplossing bij verhoogde temperatuur doet zich zonder twijfel putcorrosie voor bij roestvast staal AISI 316. Bij een stromingssnelheid van circa 12 m/s onstaat een grote hoeveelheid ondiepe putten, bij circa 1 m/s ontstaan minder putten die wel dieper zijn terwijl bij stilstand slechts enkele zeer diepe corrosieputten ontstaan. Bij hoge stromingssnelheid is ook het ontstaan van biofilms op metaaloppervlakken minder makkelijk. Bij een bepaalde stromingssnelheid zal de vorming en handhaving van een biofilm niet meer mogelijk zijn. Een eenduidige grenswaarde is gezien de tegenstrijdige onderzoeksresultaten niet te geven. Milieuzijdige inhomogeniteiten aan het metaaloppervlak zoals een bezinksellaag, afzettingen en wind-waterlijnen ontstaan eerder bij stilstand dan in een stromend medium. Hierdoor worden tijdens stilstand extra mogelijkheden gecreëerd voor het ontstaan van putcorrosie. Bij het construeren van een installatie moeten luwtes in het stromingsprofiel zoveel mogelijk worden vermeden. Ook bij leegstand van een installatie moet eraan gedacht worden dat er geen plaatsen ontstaan waar vocht kan achterblijven of opzamelen. In zeer kritische gevallen kan een speciale procedure voor buitenbedrijfstelling worden gevolgd, bijvoorbeeld droogblazen en nadien vullen met stikstof.



