Het aanpakken van rouging op RoestVast Staal
Rouging is het ongewenst rood kleuren van roestvast staal dat blootgesteld wordt aan hoog zuiver water zoals dat te zien is op afbeeldingen 1 en 2. Het ontstaat in hoog zuiver gedeïoniseerd (WFI) water boven 60℃ en ook in schone stoom (CS). WFI staat voor ‘Water For Injection’ en CS voor ‘Clean Steam’. Dergelijk water is nodig voor het produceren van bepaalde farmaceutische producten die bijvoorbeeld in het menselijk lichaam worden ingebracht.
Door Ko Buijs - Innomet Consultancy BV
(also available in English)
Het probleem rouging ontstaat meestal bij farmaceutische bedrijven en ook in mindere mate bij bedrijven in de voedingssector die met zogenaamd ‘polished water‘ werken. Deze watertypes bezitten een zogenaamd hoog ionenvacuüm omdat deze watertypen zo uitzonderlijk zuiver zijn. Het oplossend vermogen om metaalionen in dit water op te nemen is blijkbaar zo groot dat metaalatomen zelfs door de dichte chroomoxidehuid blijken te migreren richting het hoog zuivere water. Het verplaatsen van deze elementen wordt diffunderen en soms ook wel migreren genoemd. Deze ‘honger’ om stoffen op te nemen is dan ook de reden dat dit water nooit gedronken mag worden, want dat kan zelfs levensbedreigend zijn voor mens en dier. Vooral apparaten zoals fermentoren, batchtanks, mengvaten, pompen, afsluiters en bijbehorende leidingsystemen zijn inwendig gevoelig om rood te worden omdat deze worden blootgesteld aan dit type water bij hogere temperaturen. Het scheikundig mechanisme van het ontstaan van rouging verloopt als volgt:
- Fe → Fe2+ + 2e
- 2Fe + 3H2O → 2Fe(OH)3
- 2Fe(OH)3 → Fe2O3.H2O + 2H2O (boven 60oC geeft dat een rode kleur).
Austenitisch roestvast staal AISI 316L (1.4404) bestaat voor het grootste deel uit ijzer en dit element wil graag reageren met water tot ijzerhydroxide hetgeen een basische stof is. Eerst komt het ijzer als ion in het water en geeft ieder atoom twee elektronen af. Boven 60℃ converteert het ontstane ijzerhydroxide in ijzeroxide en bindt het zich aan een molecuul water. Hierdoor ontstaat een onoplosbare substantie dat neerslaat zodat het oppervlak rood gaat kleuren. Omdat het onoplosbaar is in water, maakt deze ijzerverbinding in principe geen deel meer uit van het WFI water. De weerbarstige praktijk leert ons echter dat het een utopie is dat al het ijzeroxide voor 100% neer zal slaan tot een laagje rouging. Het is daarom aannemelijk dat zeer kleine partikels van dit oxide toch verder meegevoerd worden in hetsysteem.
Food & Drugs Association
Het probleem rouging wordt gedogen door de organisatie FDA wat staat voor ‘Food & Drugs Association’. Zodra er een oplossing komt dan zal FDA deze methode nagenoeg zeker voorschrijven c.q. implementeren want rouging is en blijft een doorn in het FDA-oog. Vele wetenschappers hebben getracht dit probleem in kaart te brengen, teneinde een oplossing te vinden voor dit ongewenste fenomeen. Men heeft het gezocht in het hoger legeren van roestvast staal zoals het toepassen van duplex of 1.4435 i.p.v. 1.4404 en 904L (1.4539) alsmede in het mogelijk aanwezig zijn van deltaferriet. Al deze variabelen hebben uiteindelijk geen bijdrage geleverd om het probleem voorgoed te elimineren. Wel heeft elektrolytisch polijsten enig positief effect en dat komt vooral door de meer resistente oxidehuid die rijker is aan chroom en nikkel. De reden hiervan is dat ijzer gemakkelijker in oplossing gaat tijdens dit proces dan nikkel en chroom. Bovendien is de grootte van het oppervlak aanzienlijk kleiner geworden omdat de ‘bergen en dalen’ immers verdwenen zijn. Op deze wijze is er minder interactie mogelijk met het oppervlak, met als gevolg dat er minder rouging optreedt.
Migreren van meerdere elementen
Het grote misverstand in de praktijk is dat alleen ijzerionen in het WFI-water terechtkomen,waardoor men denkt dat het water verder geen schadelijke elementen bevat. Uit metingen is echter gebleken dat niet alleen ijzerionen in dit water terechtkomen, maar ook ionen van chroom, nikkel en molybdeen. Deze elementen zullen echter niet neerslaan maar zij zullen wel degelijk deel uitmaken van het WFI-water. Overigens gaat het om zeer kleine hoeveelheden waardoor er ook weer geen reden is voor paniek. Wel blijkt dat na een CIP-reiniging van deze systemen, er nog steeds zware metaalionen in het WFI-water achterblijven. Uiteraard is dit een ongewenste situatie. Deze ionen zijn bovendien ook niet zichtbaar en zullen dus in het WFI-water gewoon aanwezig blijven.
Na zes weken testen in WFI-water van het roestvast staal type EN 1.4435 in de aanwezigheid van lucht met daarin 1% koolzuur en stikstof, bleken de volgende hoeveelheden ionen aanwezig te zijn:
• 40 - 130 µgram ijzer per liter;
• 9 -23 µgram nikkel per liter;
• 9 µgram molybdeen per liter;
• 1 µgram chroom per liter.
Afbeelding 1: rouging in een roestvast staal AISI316 leiding en op een pompwaaier (foto’s Henkel).
De diffusie van de genoemde elementen is schematisch weergegeven in afbeelding 3. Het blauwe vlak stelt het WFI-water voor. Men ziet dat de oxidehuid uit vijf verschillende lagenbestaat die enkele nanometers dik zijn. Iedere laag heeft zijn eigen specifieke chemische samenstelling. De bovenste twee lagen bevatten geen ijzerverbindingen. Indien men een analyse maakt van roestvast staal voorzien van rouging, blijkt dat er wel ijzeratomen in de bovenste twee lagen terecht zijn gekomen. Dat is het bewijs dat er een migratie van ijzer heeft plaatsgevonden. De oxidehuid is normaal gesproken 10 – 15 nanometer dik en indien er geen ijzer in de toplaag aanwezig zou zijn, was er ook geen chroom/ijzer verhouding geweest zoals dat te zien is op afbeelding 4. Ter informatie een nanometer is 10-9. Dat betekent slechts een dikte van enige atoomlagen.
Afbeelding 2: rouging op een RVS-component.
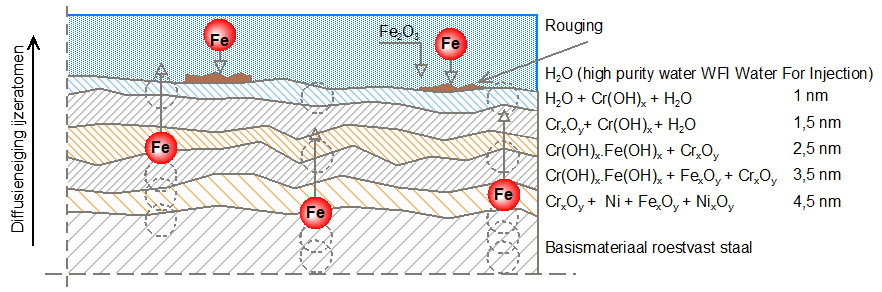
Afbeelding 3: schematische weergave van de diffusie van metaalatomen door de oxidehuid van 13 nm dik (tekening Innomet Consultancy b.v.)
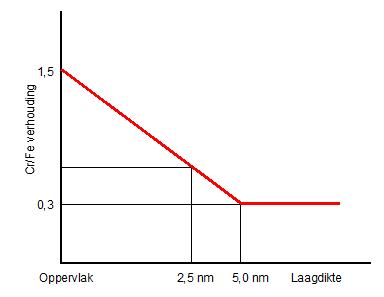
Afbeelding 4: De chroom/IJzer verhouding in de eerste 5 nanometer van de toplaag van een oxidehuid.
Daarom is het relevant dat het probleem rouging tot het verleden gaat behoren, want hoewelhet ijzer geen of weinig kwaad kan doen omdat het immers grotendeels neerslaat, heeft men wel van doen met andere metaalionen die niet in dit water thuishoren. Farmaceutische bedrijven doen aan het verwijderen van rouging en dat wordt derougen genoemd. Dat kan zowel mechanisch als chemisch plaatsvinden. Het basische ijzerhoudende deposiet is relatief eenvoudig te verwijderen door het oppervlak mechanisch te ‘wipen’, dat isechter wel arbeidsintensief. Chemisch kan dit gedaan worden met een zuur waardoor de volgende scheikundige wetmatigheid zal plaatsvinden. Die luidt: base + zuur → zout + water. Dit is ook een tijdrovend proces gevolgd door intensief naspoelen. Dat betekent tevens dat gedurende het derougen geen farmaceutische producten kunnen worden gemaakt in de betreffende installatie. M.a.w. zulke activiteiten leiden tot inkomstenderving.
Het bepalen en verwijderen van rouging
In de praktijk zijn er zogenaamde rougemeters beschikbaar die aangeven wanneer het weer tijd wordt om te gaan derougen. Dergelijke meters worden meestal in de leiding geplaatst en meten aan de hand van reflectie de intensiteit van de roodkleuring. Veelal blijkt dan dat het derougen jaarlijks moet gebeuren, hoewel het ook voorkomt dat dit om de zes maanden moet plaatsvinden. In plaats van een rougemeter, kan ook gebruik gemaakt worden van een schone witte doek die na het wrijven op het oppervlak aangeeft of derougen een noodzaak is.Tegenwoordig worden ook bemoedigende resultaten bereikt met waterige organische zoutoplossingen om de rouging te verwijderen. Dat zijn opgeloste zouten die bij hogere temperaturen gedurende vele uren actief moeten zijn om een goed resultaat te behalen. Het is echter milieuvriendelijker dan het gebruik van zuren. Daarom noemt men deze methoden ook wel bio-derougen. Al met al zal duidelijk zijn dat het ontstaan van rouge een zeer ongewenst fenomeen is. Meerdere wetenschappers en onderzoekbedrijven hebben na intensief speuren en research, internationale congressen georganiseerd om dit fenomeen de wereld uit te helpen. Vooral het bedrijf Force Technology in Denemarken heeft veel onderzoek gedaan om het ontstaan van rouging de kop in te drukken.
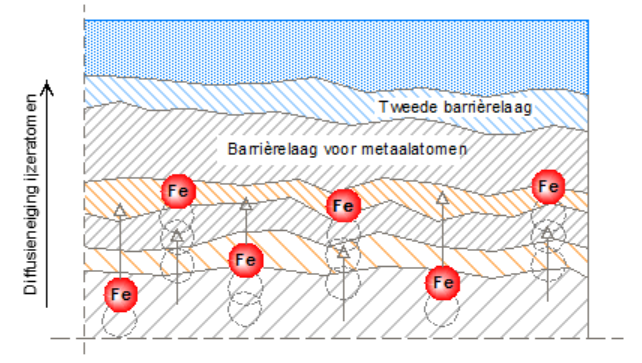
Afbeelding 5: schematisch voorstelling van de verdikte oxidehuid waardoor er een natuurlijke barrière ontstaat tegen het uitreden van metaalatomen (tekening Innomet Consultancy b.v.)
Het optimaliseren van de oxidehuid
Het bedrijf Innomet Consultancy b.v. is op het idee gekomen om de chroomoxidehuid van roestvast staal te verdikken en te verdichten m.b.v. atomaire zuurstof. Het doel hiervan is om de barrière substantieel te vergroten om het uittreden van metallische elementen tegen te gaan of zelfs geheel te voorkomen. Deze verdichting kan zowel elektrochemisch als chemisch plaatsvinden mits er maar atomaire zuurstof ontstaat. Dankzij deze verdichting en verdikking van de bovenste twee toplagen, zullen dan hoogstwaarschijnlijk de metaalatomen a.h.w. vastlopen waardoor deze a.h.w. gevangen blijven in de matrix. Deze vergroting van de barrière is schematisch weergegeven in afbeelding 5. Ook is daarbij de grootte van de verschillende metaalatomen weergegeven, wat een indicatie is over de kans dat een metaalatoom kan ontsnappen uit deze oxidehuid. Dit is schematisch weergegeven in afbeelding 6. De bedoeling is dat niet alleen ijzeratomen worden tegengehouden maar ook andere elementen die in het roestvast staal aanwezig zijn. Uiteindelijk is er een uitgebreid testprogramma opgesteld in samenwerking met een onderzoeksbureau op verschillende monsters roestvast staal. Om atomaire zuurstof te laten ontstaan, is gebruik gemaakt van ozon, waterstofperoxide alsmede anodische oxidatie. Ozon en waterstofperoxide zijn instabiele verbindingen die uiteenvallen in respectievelijk moleculaire en atomaire zuurstof alsmede water en atomaire zuurstof. Uiteindelijk bleek dat alle genoemde mediums hetzelfde effect hebben op het voorkomen van rouging. Op zich is dat logisch omdat alle mechanismen dezelfde atomaire zuurstof afgeven als oxidant.
Resultaten van het testprogramma
Er is begonnen met het testen van de roestvast staaltypen AISI304 (1.4306), 316L (1.4404), 316L (1.4435), 904L (1.4539) en duplex (1.4462). Daarvoor werden 56 monsterplaatjesgemaakt in een vierkante vorm. Deze plaatjes werden dusdanig opgehangen in het WFI-water dat een deel boven het waterniveau uitstak. Een deel van deze plaatjes werd mechanisch geslepen met K180 en een ander deel werd na dit slijpen ook nog eens elektrolytisch gepolijst. Deze monsters werden behandeld met atomaire zuurstof gedurende 24 uur bij een temperatuur van 20℃. Daarna zijn deze monsters gedompeld in WFI-water met een temperatuur van 85℃ gedurende 2000 uur. Het resultaat was dat geen enkel monster een teken van rouging vertoonde, hetgeen uiteraard een zeer positief en bemoedigend resultaat betreft.
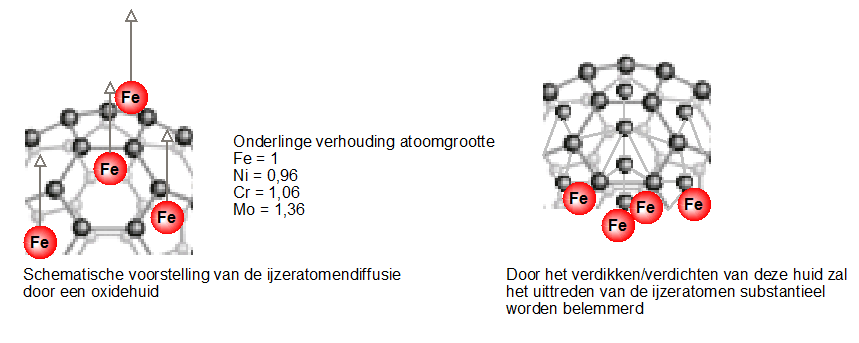
Afbeelding 6: links een ‘vrije doorgang’ voor metaalatomen en rechts een barrière door de verdikking en verdichting van de oxidehuid (tekening Innomet Consultancy b.v.)
Omdat er geen rouging ontstond bij 85℃ is besloten de temperatuur verder te verhogen naar 95℃. Deze testen in WFI-water bij deze verhoogde temperatuur omvat ook een periode van 2000 uur. Echter na 1000 uur ontstond er enige rouging op roestvast staal 304L op de overgang lucht en water. Na 2000 uur hadden alle monsters verschijnselen van rouging hoewel het monster 904L er als beste uitkwam. Blijkbaar werd met deze hogere temperatuur een kritisch kantelpunt bereikt. Dat feit is aangetoond aan de hand van het ontstaan van een nieuw evenwicht in deze oxidehuid.
Metastabiliteit
Het bleek dat de verdikte en verdichte oxidehuid bij 95℃ metastabiel bleek want het effect van de verdikking en verdichting waren verloren gegaan, waardoor er weer een normale stabiele oxidehuid was ontstaan. Het gevolg was dat rouging zich weer ging ontwikkelen zoals dat gewoonlijk ook optreedt met een natuurlijk gevormde oxidehuid. Dat is de reden dat er gezocht moest worden naar een methode om de behandelde oxidehuid dusdanig te fixeren dat deze stabiel zou blijven bij de verhoogde temperatuur van 95℃. Tot nu toe is daar nog geen oplossing voor gevonden maar wellicht is dat wel mogelijk door het oppervlak te hydrateren. De bedoeling is dan om met demiwater de verdikte oxidehuid te dusdanig fixeren opdat het een stabiel geheel kan gaan vormen. Deze behandeling kan ruwweg vergeleken worden met het hydrateren van geanodiseerd aluminium. Tijdens dit anodiseren wordt de oxidehuid aanzienlijk dikker gemaakt, maar die huid is aan het oppervlak wel poreus. Dat geeft gelijk de kans een kleurstof in deze porositeitop te laten nemen. De actie hierna is het dicht sealen van de poreuze oxidelaag en dat wordt gedaan met demiwater. De poreuze laag neemt dit water op en bindt zich aan het aluminiumoxide waardoor het opzwelt aan het oppervlak dankzij dit hydrateren. Op deze wijze verkrijgt men een dichte en dikke oxidelaag die beduidend meer corrosiebestendig is dan niet-geanodiseerd aluminium. Het lijkt logisch dat dit mechanisme ook zou kunnen werken met de verdikte en verdichte oxidehuid van het roestvast staal. Daarom zal dit een interessant onderzoek kunnen gaan worden dat uiteindelijk zal moeten leiden tot een stabiele verdikte en verdichte oxidehuid die eens en voorgoed afrekent met het probleem rouging.
Slot
Indien farmaceutische bedrijven systemen hebben die niet heter worden dan 85℃ dan is het zeker te overwegen om de componenten van roestvast staal te laten behandelen met atomaire zuurstof. Er zijn inmiddels duidelijke indicaties verkregen dat deze oxidehuid zich langdurig stabiel opstelt in tegenstelling tot een bedrijfstemperatuur van 95℃. Zoals hierboven reeds is gesteld, is het behandelen met atomaire zuurstof uitgevoerd bij een temperatuur van 20℃ gedurende 24 uur. Het zal de moeite waard zijn om deze behandeling op een aantal hogere temperaturen te laten plaatsvinden met variabele tijden. Wellicht kan dit ook een positieve bijdrage leveren aan de stabiliteit van de verdikte oxidehuid.




