Corrosieonderzoek met electrochemische-ruisanalyse
Gedurende de afgelopen dertig jaar zijn er nieuwe elektrochemische testmethodes ontwikkeld die meer en sneller informatie verschaffen over corrosiereacties. Analyse van het dynamische gedrag van een corrosiesysteem vereist speciale technieken, die essentieel afwijkend zijn van de conventionele gelijkstroomtechnieken, zoals het meten van de evenwichtspotentiaal, polarisatiekrommen, gewichtsverlies, of andere fysisch-chemische parameters. Elektrochemische-ruisanalyse is een van die nieuwe technieken.
A.J. Schornagel
Evenwichtsfluctuaties van de elektrodepotentiaal of van de celstroom worden vaak aangeduid als elektrochemische ruis, zoals dat ook wordt gedaan bij willekeurige fluctuaties in geluid of elektrische signalen. Ruisanalyse is een goed ontwikkelde techniek op velerlei gebied en wordt steeds vaker toegepast op elektrochemische systemen, in het bijzonder bij bestudering van corrosieverschijnselen. Het volgen van zowel de potentiaalfluctuaties als de stroomfluctuaties kan bijzonder nuttig blijken. Fluctuaties in de corrosiepotentiaal kunnen duiden op een verandering van de thermodynamische toestand van het corrosieproces. Fluctuaties in de stroom kunnen een aanwijzing zijn voor de corrosie kinetiek. De methode is gerelateerd aan het meten van de polarisatieweerstand Rp. Elektrochemische-ruisanalyse (ERA) kan aanwijzingen geven over het type corrosie dat gaande is en het wordt vaak gebruikt om onderscheid te kunnen maken tussen uniforme corrosie en lokale corrosie. De ernst van lokale corrosie kan worden afgeleid uit het aantal en de vorm van de ruisfluctuaties. Dit biedt een groot voordeel boven andere elektrochemische technieken. Een ander voordeel van deze meettechniek is de mogelijkheid om corrosie te volgen in milieus met een lage elektrische geleidbaarheid, bijvoorbeeld bij condensatie van dunne vochtfilms. Bovendien doen zich geen kunstmatige polarisatie effecten voor. Ruismetingen vinden plaats in de volledig natuurlijke (vrij corroderende) toestand.
Elektrochemische-ruisanalyse
De analyse van elektrochemische ruis biedt een simpele, gevoelige en vrijwel niet-destructieve meettechniek voor het vaststellen van de corrosiegevoeligheid van metalen en voor het onderzoek van corrosieprocessen. Bij het verwerken en analyseren van de elektrochemische-ruissignalen kunnen verscheidene benaderingen worden gevolgd. Er komen steeds weer nieuwe signaalanalyse methodes op. De analyse van dynamische signalen in tijdreeksen is een breed onderzocht gebied. Van een zeer geavanceerd analyse software is bekend dat het zijn oorsprong heeft in de analyse van aandelenprijzen en pogingen om die te voorspellen. Methodes die worden aanbevolen voor elektrochemische-ruissignalen omvatten onderzoek van ‘ruwe’ gegevens (met of zonder filtering), statische analyse, frequentiedomein transformatie, chao-theorie, analyse van golfpakketjes en neurale netwerken.
Meetopstelling
Met de huidige status van kennis aangaande ruisanalyse bij corrosieprocessen hoeft deze methode zich niet alleen meer te beperken tot gebruik bij experimenten in het laboratorium, maar kan ook worden gebruikt bij speciale problemen met betrekking tot het in de praktijk volgen van corrosie. Specifieke voordelen van de techniek maken dat er steeds vaker gebruik van wordt gemaakt ter ondersteuning of verbetering van conventionele corrosiebeproeving. De voordelen bestaan uit het verkrijgen van additionele informatie en verkorting van beproevingstijden. ERA is een elektrochemische methode die een groot potentieel biedt voor meten en volgen van lokale corrosie. De techniek vereist geen extern signaal om corrosiegegevens te verzamelen. Het principe berust op het feit dat twee identieke elektrodes, die worden blootgesteld aan hetzelfde medium onder vrije corrosie condities, evenwichtsfluctuaties van de evenwichtspotentiaal laten zien in het µV-gebied, hetzelfde geldt voor de galvanische koppelingsstroom in het nA-gebied, opgewekt door corrosiereacties op de elektrode-oppervlakken.
Deze potentiaal- en stroomfluctuaties staan bekend als elektrochemische ruis. De opstelling voor het meten van elektrochemische ruis is betrekkelijk eenvoudig (afbeelding 1). De twee elektrodes zijn verbonden via een ampèremeter met inwendige weerstand nul, die de ruisstroom via een multimeter geleidt naar een computer. De twee elektrodes kunnen met elkaar in serie worden verbonden via twee ultra-nauwkeurige metaalweerstanden van elk 100 kW om een gemiddeld potentiaalpunt te geven: aangezien de weerstand van de twee weerstanden veel groter is dan de weerstand van de oplossing (die in het algemeen niet hoger is dan 100 W) wordt er geen meetbare verstoring in het systeem geïntroduceerd als gevolg van de potentiaal- en stroommetingen. De potentiaal tussen dit gemiddelde punt en de referentie-elektrode (dat is bijvoorbeeld een verzadigde calomel-elektrode) wordt gemeten. Voor potentiaal- en stroommetingen bij een meetsnelheid van 2 punten/s is een meettijd van 500 s voldoende. Bij het volgen van corrosie wordt deze procedure met regelmatige intervallen herhaald.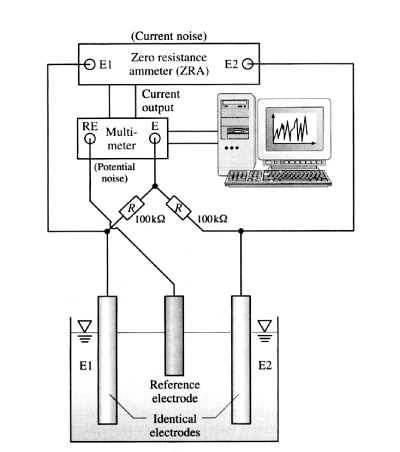
Afbeelding 1. Experimentele opstelling voor potentiaal- en stroomruis metingen.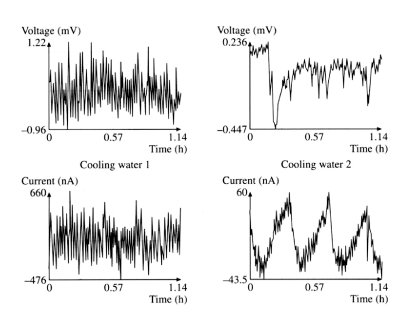
Afbeelding 2. Potentiaal- en stroomruis bij koolstofstaal in verschillende koelwatersoorten [1].
Interpretatie
Afbeelding 2 toont potentiaal- en stroomruis als functie van de tijd voor koolstofstaal in twee verschillende oplossingen van zout in koelwater. Koelwater 2 bevat een wat hogere concentratie chloride en sulfaat, hetgeen resulteert in een aanzienlijk ander fluctuatiepatroon van de elektrochemische ruis aan het staal in dit watertype. De elektrochemische ruissignalen kunnen zowel analoog als digitaal worden verwerkt. De digitale signaalbewerkingstechniek bestaat uit verzamelingen van gegevens en hun daaropvolgende numerieke analyse, terwijl de analoge verwerkingsmethode met behulp van filters en versterkers een uitgangssignaal levert dat evenredig is met het kwadratisch gemiddelde van de ruis. De vermogensspectraaldichtheid bij hoge frequenties (100 - 1000 MHz) kan een aanwijzing zijn voor algemene corrosie. De vorm en de repetitiesnelheid van de sprongen van de elektrochemische potentiaal en stroom bepalen het type corrosie. De helling van de vermogensspectraaldichtheid van de elektrochemische spanningsruis curve, na verwijdering van de lineaire trend, bleek een significante parameter te zijn voor het onderscheiden tussen uniforme en lokale corrosie. De elektrochemische ruis die wordt voortgebracht door uniforme corrosie heeft een vrijwel uniform frequentiespectrum en daarom is de helling vrijwel nul. Elektrochemische ruis, voortgebracht door lokale corrosie, bestaat uit exponentieel dalende sprongen en de helling van de vermogensspectraaldichtheid curve is hoger [> 12 dB(V2Hz-1)]/decade. Afbeelding 3 toont vermogensspectraaldichtheid-curven die, voor het uniform corroderende staal in koelwater 1, een helling hebben van 6,3 dB(V2Hz-1)/decade, terwijl voor het lokaal corroderende staal in koelwater 2 deze helling 15,3 dB(V2Hz-1)]/decade bedraagt.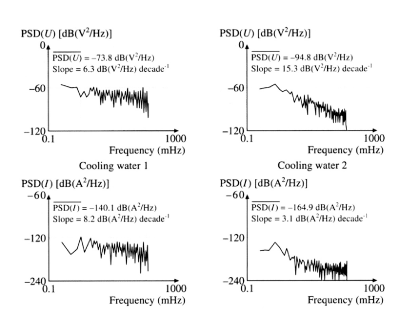
Afbeelding 3. Vermogens-spectraaldichtheid (Engels: Power Spectral Density of PSD) spectra voor koolstofstaal in verschillende koelwatersoorten [1].
Het alleen meten van potentiaalruis kan misleidende resultaten opleveren in gevallen waarbij kleine fluctuaties in massa transport grote veranderingen kunnen geven in de corrosiepotentiaal. Dat is het geval bij metalen en legeringen die immuun zijn voor corrosie (zoals platina) of die passief zijn (zoals roestvast staal) in neutrale, beluchte waterige oplossingen. De verklaring moet worden gezocht in het massatransport van zuurstof, dat een grote rol speelt bij potentiaalruis. Voor het volgen van corrosieverschijnselen heeft statistische analyse van ruisgegevens, resulterend in kwadratische gemiddelden, tal van voordelen boven spectraalanalyse, welke laatste dure apparatuur en/of gecompliceerde analyseprogramma’s vereist. Er is aangetoond dat de ruisweerstand Rruis en de polarisatieweerstand Rp overeenkomstige waarden en trends hebben. Dus voor die gevallen waar alleen op een snelle en goedkope manier verkregen kwalitatieve resultaten nodig zijn, is het verzamelen en evalueren van Rruis gegevens voldoende. Een kwantitatief begrip van elektrochemische ruis en zijn relatie met corrosie, met name met lokale corrosieverschijnselen, kan alleen worden verkregen via spectraalanalyse van ruisgegevens, hetgeen leidt tot de bepaling van de spectraal-ruisweerstand RSruis, die sterke relatie vertoont met Rruis en Rp.
Praktijkgeval
Er is onderzoek gedaan [2] naar de invloed van mangaan- en ijzersulfide insluitsels in roestvast staal in onbeluchte en beluchte 3% NaCl-oplossingen. Indien dergelijke insluitsels zich aan het staaloppervlak bevinden, kunnen ze plaatselijk de passieve laag nadelig beïnvloeden en als kiemplaats fungeren voor putcorrosie. Er zijn een viertal staaltypen onderzocht waarvan de chemische samenstelling is weergegeven in tabel 1. Omdat het in oplossing gaan van MnS en FeS plaatsvindt bij de evenwichtspotentiaal van roestvast staal, kan er gebruik worden gemaakt van voor het volgen van deze verschijnselen van ERA. Tabel 2 geeft een samenvatting van de potentiaal-tijd gegevens in de vorm van een gemiddeld aantal pieken, de gemiddelde spronggrootte, het gesommeerde piekoppervlak (V.s), de gemiddelde corrosiepotentiaal Erp.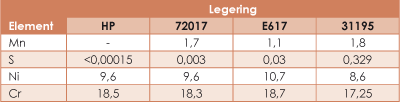
Tabel 1. Samenstelling RVS-legeringen.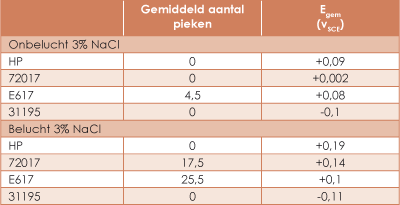
Tabel 2. Samengevatte ERA-gegevens voor vier 18-8 legeringen in onbeluchte en beluchte 3% NaCl-oplossingen.
Expositie in onbeluchte oplossing
Gegeven de geringe beschikbare hoeveelheid zuurstof in de onbeluchte elektrolyt is een andere kathodische reactant noodzakelijk om corrosie op gang te brengen. De vrije corrosiepotentiaal van het staal bevestigt dit. De hoogzuivere legering met minder dan 0,0015% S waarvan ideaal gedrag mag worden verwacht gaf een Ecorr te zien van +0,09 VSCE. Dit is een waarde die overeenkomt met de mengpotentiaal van de elektrolyt de zogenaamde redoxpotentiaal en heeft niets van doen met corrosiegerelateerde processen. De legering met een gemiddeld zwavelgehalte E617 gaf enkele sprongen te zien. De kathodische reactie komt voort uit de zeer geringe hoeveelheid zuurstof die toch nog in de oplossing aanwezig is ondanks het ontluchten en ook afkomstig van protonen die worden gevormd tijdens lokale oplossing van de insluitsels. De vrije corrosiepotentiaal van E617 bedroeg +80 mVSCE, hetgeen wijst op een nagenoeg passieve toestand. De legering met het hoogste zwavelgehalte 31195 vertoonde aanvankelijk gedurende enkele seconden een potentiaal van ongeveer +0,19 VSCE, die echter snel daalde naar een constante waarde van -100 mVSCE, hetgeen wees op een snelle depassivering. Er werden bij legering 31195 geen sprongen waargenomen. Dus de hoogzuivere legering HP, die steeds volledig passief was en legering 31195, die volledig was gedepassiveerd, gaven geen sprongen te zien, waaruit kan worden geconcludeerd dat niet uitsluitend mag worden vertrouwd op het aantal sprongen als aanwijzing voor de mate van putinitiatie.
Expositie in beluchte oplossing
Onder beluchte omstandigheden werd aanvankelijk aangenomen dat in alle gevallen zuurstof de belangrijkste kathodische reactant was. Al het oplossen vond plaats met een hogere snelheid hetgeen tot uitdrukking kwam in de potentiaalsprong verdeling voor E617 met 25,5 sprongen per opgenomen tijdsperiode, dit in tegenstelling met de 4,5 sprongen in onbelucht milieu. De waarde van Ecorr steeg naar bijna +0,2 VSCE voor de passieve legering HP (afbeelding 4) en varieerde in overeenstemming met insluitsel type en hoeveelheid in de andere legeringen. Hoe kleiner het aantal insluitsels des te hoger was de repassiveringspotentiaal Rrep. Legering 31195 werd weer gedepassiveerd van een beginwaarde van +0,19 VSCE naar -0,11 VSCE (afbeelding 4) ondanks de aanwezigheid van zuurstof. Ook nu weer vertoonden HP en 31195 potentiaalsprongen en wel om dezelfde redenen als bij expositie in de onbeluchte oplossing. Legering E617 vertoonde echter toegenomen ruis in termen van aantal, maximale potentiaalverplaatsingen en potentiaal/tijd integralen. In aanwezigheid van zuurstof bleek legering 72017 in staat tot depassivering, hetgeen niet het geval was onder onbeluchte condities.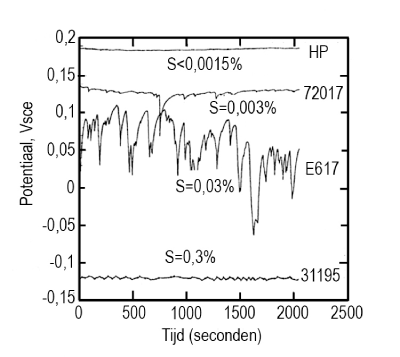
Afbeelding 4. Potentiaal-tijdopname voor vier 18-8 RVS-legeringen in belucht 3% NaCl [2].
Referenties
1. A. Legat. Electrochemical Noise as the basis of corrosion monitoring, 12th Int. Corrosion Congress 3A(1993) p. 1410 - 1419.
2. N.J.E. Dowling, C. Thual-Duret, G. Auclair, J.P. Auduard, P. Combrade. Assessment of the Pitting Susceptibility of AISI 303 and 304 Stainless Steels as a Function of Sulphur Content Using Electrochemical Noise. Progress in the Understanding and Prevention of Corrosion. Vol.2. Institute of Metals, 1993, p. 1328 - 1339.



