De kunst van het passief overleven
Soms baal ik werkelijk van die passieve mensen, languit en lamlendig in de zetel liggend of achterover hangend op een stoel die ieder moment achterover dreigt te slaan. Was het niet dat dat serieus pijnlijk voor de lamlendige kan zijn, ik zou het bijna hilarisch vinden mocht dat effectief gebeuren. Ze zagen erop los over de vermeende lamentabele staat van de wereld, over de koetjes die niet willen kalven en, éénmaal ze er zijn, over de kalfjes die niet in de richting van de zeurder’s ideeën en gedachten willen lopen. Er mee iets aan doen, ho maar, dat is teveel gevraagd nu ze zich nog eens extra in hun dekentje wentelen of een geruite plaid over hun kouwelijke benen draperen.
© Frans Vos, General Manager Materials Consult bv
Nee, geef mij dan maar het actieve leven, dat van het eigen steentje aan de wereld proberen bij te dragen. Niet altijd gemakkelijk, dat geef ik gaarne toe, maar liever positief actief in de wereld staan dan tot het gilde van de Zure, Zeurende Zagers, de ZZZ-club, toe te treden.
Met voorgaande uithaal naar de passieve ZZZ-mentaliteit, krijg ik echter een dubbel, zelfs bijna een hypocriet gevoel. Een groot deel van mijn professionele leven ben ik immers bezig met een positieve boodschap over het passieve in de wereld uit te dragen. Ik kan er nu eenmaal niet omheen: Als het gaat over de strijd tegen corrosie is passiviteit een zegen.
Aluminium, roestvast staal en ook verschillende klassiekere staalsoorten, bv. Cortenstaal, danken hun leven aan passiviteit of, beter uitgedrukt, aan de aanwezigheid van een zogenaamde ‘passivatielaag’ op hun oppervlak. In mijn gedachten zie ik sommigen onder u al steigeren nu ik het lef heb om Cortenstaal passiviteit toe te dichten, maar laat me toch even toe om één en ander verder te verklaren en te nuanceren.
Zij die meer over de passivatielagen van metalen willen te weten komen, vinden een eerste bondgenoot in wijlen prof. Pourbaix van de ULB, de Université Libre de Bruxelles. Prof. Pourbaix ontwikkelde de in de corrosiewereld wereldberoemde ‘E-pH diagrammen’. Met deze ‘Pourbaixdiagrammen’ wordt getracht om voor een bepaald metaal dat wordt blootgesteld aan een bepaalde omgeving te voorspellen of het betreffende metaal zal corroderen, ‘of’ dat er een beschermende metaaloxide- of hydroxidelaag zal worden gevormd op het metaaloppervlak ‘of’ dat er helemaal niets zal gebeuren met het metaal, ook wel als ‘immuniteit’ omschreven.
Welke van deze drie mogelijkheden zich voordoet, wordt daarbij gekoppeld aan de in het corrosiesysteem aan het metaaloppervlak heersende potentiaal (E) en de zuurtegraad (pH) van het milieu dat met het metaal in contact staat.
Aangezien mijn doel het behouden van uw aandacht is, ga ik u de volledige theoretische uitleg besparen (de uitgever wenst bovendien ook nog andere leeswaardige artikels onder uw aandacht te brengen), maar laat me toe even één en ander met een concreet voorbeeld te illustreren.
Hieronder ziet u het vereenvoudigd Pourbaixdiagram voor zuiver ijzer in zuiver water bij kamertemperatuur en bij omgevingsdruk. Een eerste vaststelling: Om dat diagram te mogen gebruiken, zijn er al heel wat randvoorwaarden: het metaal (ijzer), het milieu (zuiver water), temperatuur (20 à 25°C) en omgevingsdruk (1 atmosfeer, wat ongeveer 1 bar is, 1.013249966 bar om iets meer precies te zijn). 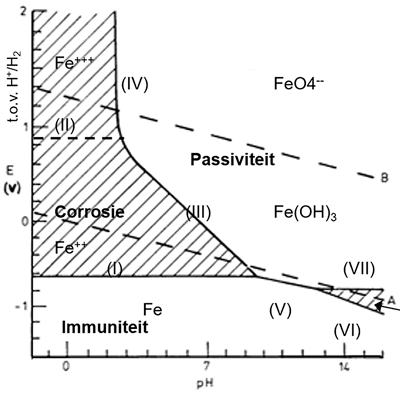
Weinig praktisch lijkt het wel, want wie gebruikt er nu zuiver ijzer in zuiver water? Gelukkig is er nog het pragmatisme, aan wie we het te danken hebben dat we dit diagram ook wel als benadering voor ongelegeerde staalsoorten, zelfs voor sommige laaggelegeerde staalsoorten kunnen gebruiken. Dit diagram gebruiken voor bv. Cortenstaal of roestvast stalen is echter uit den boze; hun chemische samenstellingen wijken immers te ver af van ‘zuiver ijzer’ en dus is de boodschap dat je voor de gedragsstudie van Cortenstaal en roestvast stalen andere E-pH diagrammen moet gebruiken. Idem als je het corrosiegedrag in andere omgevingen dan zuiver water wil bestuderen. Ook voor studies van het corrosiegedrag in zeewater, afvalwater, grondwater enz. kan u dus uw queeste naar de daarvoor geldende Pourbaixdiagrammen alvast starten, om dan over de temperaturen nog te zwijgen.
De volgende stap: Het bepalen van de potentiaal en de zuurtegraad. Dat laatste is op zich niet zo moeilijk. Voor het meten van de pH zijn er allerhande meetmethoden beschikbaar, gaande van de eenvoudige, maar benaderende indicatorstrips, over labometers in allerhande maten en gewichten tot een heuse titratie. Ook het bepalen van de potentiaal – jawel, de elektrische; corrosie is niet voor niets ‘elektro’chemie – is op zich niet zo moeilijk als je naast een referentie-elektrode ook een Voltmeter met milli- en microschalen ter beschikking hebt.
Als je dan potentiaal E en zuurtegraad pH kent, kan je op basis van het Pourbaixdiagram inschatten of het metaal in een staat van immuniteit, passiviteit of corrosie belandt.
In waterige omgevingen bij kamertemperatuur en atmosferische druk is het bekomen van immuniteit bij stalen veelal utopie; de potentiaal is quasi steeds te hoog voor immuniteit. Voor stalen eindig je dus bij ‘corrosie’ ofwel bij ‘passiviteit’. Nu, één van de grootste misvattingen bij niet-ingewijden is dat de creatie van een passivatielaag automatisch impliceert dat er geen corrosie meer zou zijn. Zij dwalen. Passivatielagen zijn in wezen niet meer en niet minder dan ‘roest’lagen met de extra twist dat zij zich egaal en gelijkmatig over het metaaloppervlak ontwikkelen. Zoals ik al in menige andere publicatie heb geduid, is roest geen corrosie, maar wel een mogelijk gevolg van corrosie. Zonder corrosie kan je dus ook geen roest en dus evenmin passivatielagen krijgen. Wat Pourbaix in zijn diagrammen aangeeft, is dus niet de grens tussen wel of geen corrosie, maar wel de grens tussen het optreden van ongebreidelde, veelal lokale corrosie en het optreden van een uniforme corrosie waarbij tegelijk de egale, gelijkmatige passivatielaag wordt gevormd. Tegelijk geven de corrosie-passiviteit grenzen op Pourbaixdiagrammen de overgang aan tussen een inspecteerbare, controleerbare, beheersbare situatie bij de vorming van de passivatielaag en een veel moeilijker beheersbare en veel moeilijker inspecteerbare situatie als er geen passivatielaag wordt gevormd.
Afhankelijk van de metaalsamenstelling, de omstandigheden (milieu, temperatuur, druk, …) enz. kan het een laag zijn die quasi impermeabel is voor chemische stoffen, maar er kan evenzeer nog sprake zijn van een bepaalde mate van permeabiliteit, waardoor aan het grensvlak tussen de passivatielaag en het metaal de corrosie in een uniform regime kan verder schrijden. ‘Permeabiliteit voor chemische stoffen’ kan daarbij diverse betekenissen hebben en slaan op diverse substanties (water, zuurstof, waterstof, diverse types ionen, …). Een verdere uitleg zou mij hier echter veel te ver leiden, maar de belangrijkste boodschap is dat zich aan het grensvlak tussen metaal en passivatielaag wel degelijk nog reacties kunnen voordoen die het metaal in een component of componenten van de passivatielaag omzetten, dus tot metaalverlies leiden.
Als we dan bij wijze van voorbeeld enkele metaalfamilies vergelijken, vertonen passivatielagen op aluminiumlegeringen in vele industriële en bouwkundige toepassingen een hoge tot zeer hoge impermeabiliteit. De impermeabiliteit van de passivatielagen op roestvast stalen is in vele toepassingen evenzeer hoog, maar toch al ietwat minder vergeleken met aluminiumlegeringen. Ook bij weerbestendige stalen zoals bv. Cortenstaal speelt de vorming van een passivatielaag een belangrijke rol in het beheersbaar/controleerbaar houden van de corrosie, maar de passivatielagen op de meerderheid van de weerbestendige stalen vertonen wel nog een permeabiliteit die merkelijk hoger is dan bij aluminium en roestvast stalen. 
Courtesy the Resonant Sculpture Project, Saxophonist: Avram Fefer, Sculptures: Richard Serra.
Als deze prachtige Cortenstalen sculpturen in een propere, maar vochtige omgeving zouden worden tentoongesteld, zullen ze met andere woorden sneller verdwijnen dan dat ze met dezelfde plaatdiktes uit een roestvast staal of aluminium zouden zijn vervaardigd.
Passivatie betekent dus duidelijk niet hetzelfde als ‘de corrosiesnelheid is gelijk aan nul’. Zij die nog niet (helemaal) zijn overtuigd nodig ik uit om eens in de studie van de zogenaamde ‘polarisatiecurven’ te duiken en, eenmaal je weet wat daaruit valt af te leiden, enkele curves voor verschillende metaallegeringen in gelijkaardige blootstellingscondities te vergelijken.
Het feit dat met de creatie van een passivatielaag de situatie beter beheersbaar en controleerbaar wordt, geeft tegelijk ook het enorme belang aan van de instandhouding van de passivatielaag. Bij het geheel of zelfs maar lokaal verdwijnen van de passivatielaag gaan de poppen aan het dansen en valt de bescherming tegen een ongebreidelde, al dan niet lokale corrosie weg. Met graagte deel ik met u enkele van de vele voorbeelden uit mijn dagelijkse schade-analyse praktijk.
Zo is er het bijzonder trieste verhaal van het echtpaar dat enkele weken na het vullen van de stookolietank werd geconfronteerd met de vaststelling dat een groot gedeelte van de stookolie niet meer in de tank, maar wel in de grond rond de tank was terecht gekomen. De schuldige was niet de tank zelf, maar de terugloopleiding die was afgebroken net boven de aansluiting met de stookolietank. In het betreffende installatietype werd een overmaat aan brandstof naar de brander gepompt, waarbij het overtollig deel via een terugloopleiding terug naar de tank werd geleid. De leidingen tussen brander en tank waren daarbij uitgevoerd in flexibele leidingen van met kunststof bekleed aluminium. Voor de aankoppeling met de tank moest de kunststofbekleding echter over een klein stukje worden verwijderd om een goede aansluiting in het koppelstuk te bekomen, enigszins vergelijkbaar met het afstrippen van de bekleding van een elektriciteitsdraad als je bijvoorbeeld een stopcontact wil aansluiten. Ter hoogte van de aansluiting van de terugloopleiding was de kunststoffen bekleding echter te ver weggenomen, waardoor een gedeelte van de aluminium leiding ook buiten het aansluitblok onbekleed was. In normale omstandigheden had de gebruikte aluminiumlegering daar niet al te veel hinder van mogen ondervinden en zijn passivatie moeten behouden. Volgens het in deze omstandigheden geldende Pourbaixdiagram is de passivatielaag op aluminiumlegeringen immers stabiel bij pH-waarden tussen 4 en 8. Onder een pH van 4 en boven 8 wordt de passivatielaag echter instabiel. De verwachte stabiliteit van de passivatielaag was daarbij in het gedrang gekomen door werkzaamheden aan de oprit van het huis. Enkele maanden voor het falen had het echtpaar beslist het niveau van de oprit te laten verhogen. De aannemer had daarbij de bakstenen toegangsput tot de aansluitingen en vulopening van de stookolietank echter niet opgemetseld tot het nieuwe opritniveau, waardoor bovenaan de toegangsput geen bakstenen, maar enkel afgestreken ‘stabilisé’ aanwezig was. Stabilisé is een zandmengeling die wordt gebruikt als onder- en stabilisatielaag bij onder andere klinkerwerken, maar aan die mengeling is ook cement toegevoegd. En bij dat cement zit het addertje onder het gras. In vochtige omstandigheden stijgt de pH van cementhoudende zandmengsels in vele gevallen tot boven de 8. Rest nog de vraag hoe dat aluminium onderaan de toegangsput in contact was gekomen met de stabilisé? Wel, omdat de put niet was opgemetseld bij het verhogen van de oprit en de stabilisé tussen de rand van het bakstenen gedeelte en de klinkers van de nieuwe oprit onvoldoende was gecompacteerd, was een gedeelte van de stabilisé in de put en rond de te ver afgestripte terugloopleiding beland. De gevolgen waren niet te overzien. Een verplichte bodemsanering van een groot gedeelte van hun eigen grond en ook nog eens een deel bij de buren. Ik hoop van harte dat een verzekeraar de kosten heeft vergoed, want voor een particulier is dat anders niet te betalen.
Voor het tweede voorbeeld gaan we voor een klassieker: De veelal nefaste gevolgen van onder andere chloride-, fluoride-, sulfide- en sulfaationen, op de stabiliteit van de passivatielagen op roestvast stalen van de AISI 304 familie en, afhankelijk van de concrete omstandigheden, soms ook op hoger gelegeerde roestvast stalen. Vanuit het perspectief van de betreffende Pourbaixdiagrammen brengt de afzetting van dergelijke ionen op roestvast stalen een verlaging van de potentiaal met zich mee, waardoor ter hoogte van de ionische afzetting de passivatiebescherming op de proef zal worden gesteld. Voor zij die de moed hebben of al hadden om de studie van polarisatiediagrammen ter harte te nemen, vertaalt zich dat o.a. in een verlaging van de ‘putcorrosiepotentiaal’. In redelijk wat situaties is het dan de gewoonte om over te schakelen naar een molybdeenhoudend roestvast staal uit de AISI 316 familie, maar dat is niet altijd voldoende en is het gebruik van nog hoger gelegeerde roestvast stalen of het overstappen naar een andere metaalfamilie aan te bevelen. Het risico op een destabilisatie van de passivatielaag wordt uiteraard bepaald door nog heel wat meer parameters dan het metaaltype en de afzetting van die vervelende ionentypes alleen. Een verhoogde aanwezigheid van ionen in de met het metaal in contact staande omgeving impliceert immers ook een verhoogde geleidbaarheid van de elektrolyt (meestal water), wat op zich ook nog een invloed heeft. Temperatuur, druk, de eventuele aanwezigheid van kalk- en andere afzettingen enz. enz. bepalen mee of al dan niet corrosie zal optreden.
Corrosie is immers geen materiaaleigenschap, maar een systeemeigenschap. Systeemdenken is de sleutel om corrosie te begrijpen en haar te vermijden of, als vermijden niet tot de mogelijkheden behoort, haar onder controle te houden.
En zo komt uw actieve leesfase van dit artikel bijna tot een einde. U bent niet in een passieve status belandt, waarvoor mijn bijzondere dank. Corrosie is weliswaar een alledaags, maar helaas geen gemakkelijk uit te leggen fenomeen. Ik zou het u dus zeker niet kwalijk nemen als u inmiddels de draad zou zijn verloren.
Tot slot, toch nog één bijzonder voorbeeld van positieve passivatie die naar mijn volledig persoonlijke mening zowel u persoonlijk, uw naasten als iedereen die u ontmoet ten goede zal komen: Uw coronavaccinatie.
Toegegeven, net zoals een passivatielaag niet 100% impermeabel is, biedt ook vaccinatie geen 100% zekerheid dat we nooit persoonlijk door een covidbesmetting zullen worden getroffen. Persoonlijk verkies ik echter die niet-100% zekerheid boven de 100% zekerheid dat ik niet beschermd ben als ik me niet laat vaccineren. Bovendien zorg ik er met mijn vaccinatie ook voor dat alle medemensen die ik op mijn pad tegenkom een beetje extra zijn beschermd. Elkaar beschermen, is dat niet ieders taak in het samenleven?
De parallel tussen de passivatielagen in de metaalkundige wereld en onze eigen coronavaccinatie is een duurzaam leven!




